Clear Sky Science · ar
تحفيز لاكتلة ZEB2 عبر مسار التحلل السكري KDM6B/Pdk1 يعزز تكوّن الأسمنت الخلوي
لماذا حماية جذور الأسنان مهمة
أمراض اللثة، أو التهاب دواعم السن، تُعدّ من الأسباب الرئيسية لفقدان الأسنان لدى البالغين. مع تقدّم المرض، تتآكل بصمت الأنسجة التي تثبت الأسنان في الفك. من أهم هذه الأنسجة الأسمنت، وهو طبقة رقيقة شبيهة بالعظم تغطي سطح الجذر وتسمح للسنة بالارتباط بالرباط والعظم المحيط. بمجرد فقدان الأسمنت، تزداد ارتخاء الأسنان وقد تتساقط في النهاية. تطرح هذه الدراسة سؤالاً بسيطاً لكنه ذا أثر: هل يمكننا فهم كيفية بناء الأسمنت على مستوى جزيئي بحيث نتمكن في المستقبل من مساعدة الجسم على إعادة بنائه وإبقاء الأسنان في مكانها مدى الحياة؟
من الخلايا الداعمة للأسنان إلى هدف علاجي
يصنع الأسمنت خلايا متخصصة تُسمى الأمينتوبلاستات، التي تجلس على سطح الجذر وتودع مادة معدنية جديدة. تتصرف هذه الخلايا بشكل مشابه لخلايا تكون العظم، لكن الإشارات التي تخبرها متى وكيف تبني الأسمنت كانت مفهومة بشكل سيئ. ركّز الباحثون على جزيء يسمى KDM6B، إنزيم يحرر علامات كيميائية عن بروتينات تغليف الحمض النووي ويمكنه تشغيل الجينات. من خلال دراسة أسنان الفئران في أعمار مختلفة والأمينتوبلاستات المزروعة مختبرياً، وجدوا أن مستويات KDM6B ترتفع خلال مرحلة النشاط في تكوين الأسمنت وتنخفض بعد تباطؤ النمو. عندما أعاقوا KDM6B في الخلايا أو في الفئران، انخفض نشاط الأمينتوبلاست وبات الجزء "الخَلَوي" من الأسمنت — الجزء السميك والحيوي قرب قمة الجذر — أرفع، ما يشير إلى أن KDM6B يعمل كمحفز رئيسي لنمو أسمنت صحي.
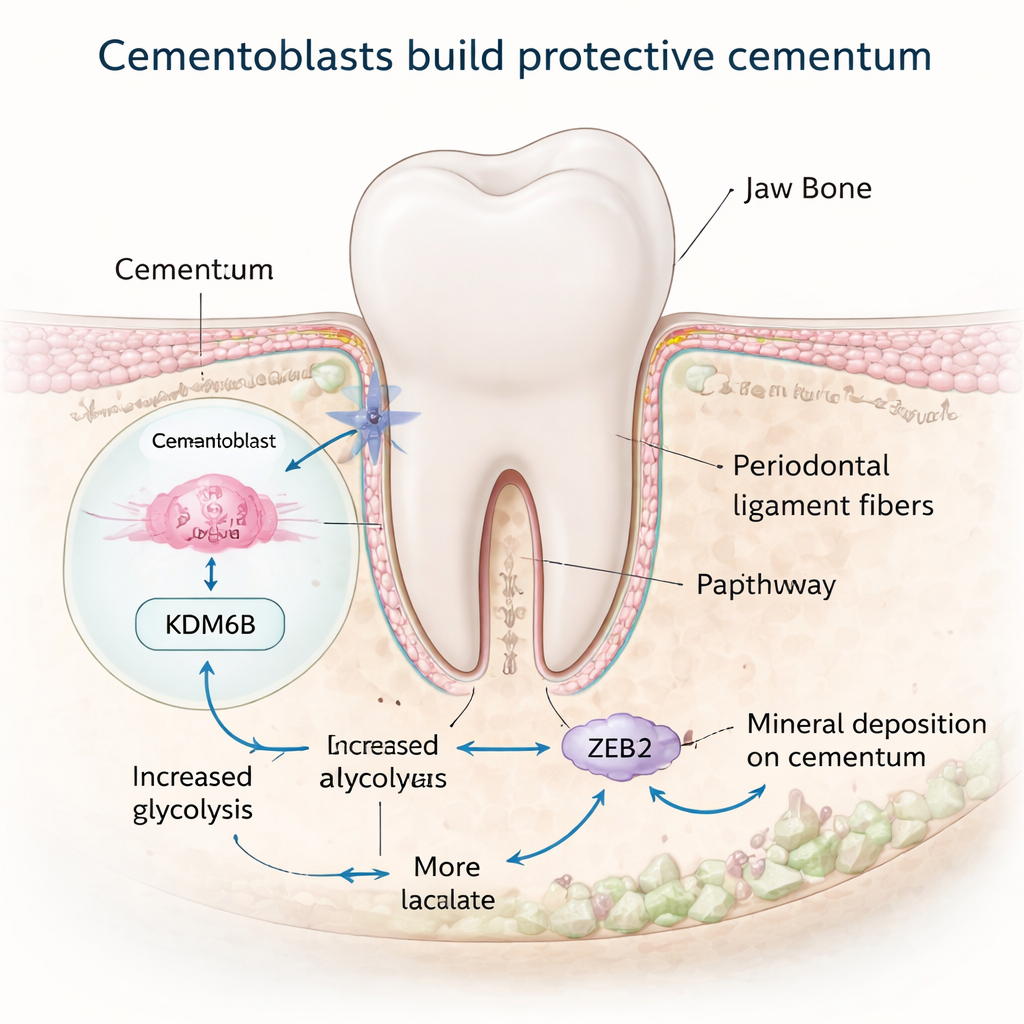
إعادة توصيل تمثيل الخلايا للطاقة لبناء النسيج المعدني
بناء نسيج مُكلّس يتطلب طاقة عالية، وتنتقل العديد من الخلايا إلى حالة تمثيلية عالية الأداء أثناء ذلك. اكتشف الفريق أن KDM6B يساعد الأمينتوبلاستات على إعادة توصيل طريقة استخدام السكر. عادةً تفضل هذه الخلايا مساراً يُسمى التحلل السكري، الذي يكسر الجلوكوز بسرعة وينتج لاكتات. عندما قلَّ KDM6B، انخفضَ تعبير الجينات المشاركة في التحلل السكري، بينما تحوّلت أو ارتفعت الجينات المرتبطة بإنتاج طاقة أبطأ واعتمادًا على الأكسجين، وصنعت الخلايا طاقة أقل إجمالاً. لاعب محوري في هذا التحوّل كان إنزيم يدعى PDK1. باستخدام أدوات رسم الخريطة الجينومية، أظهر الباحثون أن KDM6B يزيل فعلياً علامة كابحة من منطقة الحمض النووي التي تتحكم في جين Pdk1، مما يسمح بارتفاع مستويات PDK1. إعادة PDK1 في خلايا ناقصة KDM6B أعادت العديد من علامات التكلّس، كاشفة عن مفتاح أيضي KDM6B–PDK1 يغذي الأمينتوبلاستات.
تحويل اللاكتات من نفاية إلى إشارة نافعة
غالباً ما يُنظر إلى اللاكتات كمنتج نفاية للعضلات المجهدة، لكن أعمال حديثة أظهرت أنه يمكن أن يعمل أيضاً كإشارة تعدّل البروتينات. هنا، زاد التحلل السكري الأعلى المدفوع بـKDM6B وPDK1 إنتاج اللاكتات في الأمينتوبلاستات. تتبّع الباحثون بعدها نمط تعديل بروتين جديد يسمى اللاكتلة (lactylation)، حيث تُلحق علامات مشتقة من اللاكتات بمواقع محددة على البروتينات. وجدوا أن مستويات اللاكتلة في الأمينتوبلاستات ارتفعت خلال فترات تكوين الأسمنت النشط وانخفضت في الفئران الأكبر سنًا وفي الخلايا الناقصة KDM6B. إضافة لاكتات الصوديوم أعادت رفع اللاكتلة، ونشطت جينات متعلقة بالتكلّس، واستعادت تكون عقيدات معدنية في الخلايا المزروعة وفي نموذج فأر، حتى عندما كان KDM6B محجوباً. هذا يشير إلى أن اللاكتات نفسها يمكن أن تساعد في إنعاش نشاط بناء الأسمنت الضعيف.
دفع جزيئي لمُنظّم أساسي للأسمنت
سأل الفريق بعد ذلك أي البروتينات تُزَيَّن باللاكتلة بطريقة مهمة للأسمنت. ركّزوا على ZEB2، بروتين منظم للجينات معروف سابقاً بتعزيز تكلّس الأمينتوبلاستات. باستخدام تقنيات رسم البروتينات، حدّدوا مواقع محددة على ZEB2 تحمل علامات لاكتلة وأظهروا أن تعديل موقع حاسم واحد أضعف قدرة الخلية على تشغيل جينات التكلّس. أظهرت تجارب إضافية أن مسار KDM6B–PDK1 يعزز لاكتلة ZEB2 وأن تزويد الخلايا بلاكتات إضافية يمكن أن يعيد نشاط ZEB2 حين يكون PDK1 منخفضاً. جوهرياً، يربط هذا بين الأيض والتحكم بالجينات: يكسر تحلل السكر الجلوكوز ليولد لاكتات، والتي تضبط ZEB2 كي تستمر برامج بناء الأسمنت بقوة.
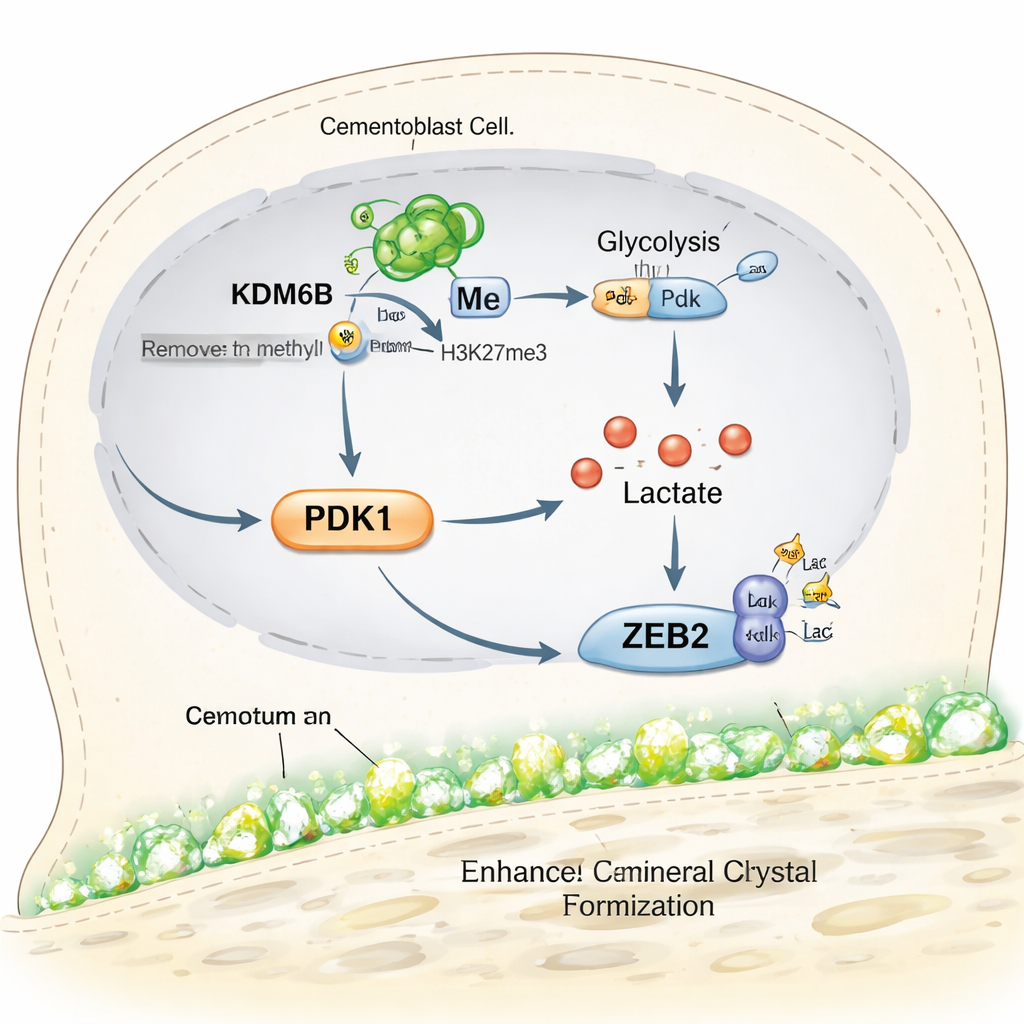
ما يعنيه هذا للعلاجات المستقبلية لإنقاذ الأسنان
ببساطة، تكشف الدراسة سلسلة من الأحداث داخل خلايا مكوّنة للأسمنت: يفتح إنزيم KDM6B جين Pdk1، يدفع PDK1 الخلايا نحو استخدام سكر سريع، هذا الاستقلاب يولّد لاكتات، واللاكتات تضبط كيميائياً بروتين ZEB2 لدفع ترسيب المعادن. عندما يتعرقل أي رابط في هذه السلسلة، يتراجع نمو الأسمنت، لكن إضافة لاكتات محكمة يمكن أن تعيده جزئياً. بالنسبة للمرضى، لا يترجم هذا العمل بعد إلى علاج سريري فوري، لكنه يبرز أهدافاً دقيقة جديدة للأدوية أو المواد الحيوية المصمَّمة لتجديد الأسمنت وتثبيت الأسنان في حالات التهاب اللثة المتقدّم. كما يقترح أن مفاتيح أيضية مماثلة قد تُستخدم لتشجيع شفاء العظام في أماكن أخرى من الجسم.
الاستشهاد: Yang, Z., Wang, H., Xiao, J. et al. KDM6B/Pdk1 glycolytic pathway-driven ZEB2 lactylation promotes cellular cementum formation. Int J Oral Sci 18, 21 (2026). https://doi.org/10.1038/s41368-025-00420-5
الكلمات المفتاحية: تجديد الأسمنت, التهاب دواعم السن, تمثّل خلايا الأمينتوبلاست (cementoblast), مزيل مثيلة الهستون KDM6B, لاكتلة البروتين