Clear Sky Science · ar
رؤى هيكلية في الطفرات المرتبطة بالأمراض في آلية معالجة الميكرو RNA
كيف تشكل مقصات الحمض النووي الريبي الدقيقة الصحة والمرض
داخل كل خلية، يعمل نظام تعديل خفي يقلم الرسائل الجينية قبل أن تُقَرأ. يعتمد هذا النظام على قصاصات حمض نووي ريبي صغيرة تُسمى الميكروRNA، التي تعمل كمقابض ضبط دقيقة لآلاف الجينات في آن واحد. عندما تعمل «الآلات» الجزيئية التي تصنع الميكروRNA بالشكل الصحيح، تنمو الخلايا وتنقسم وتتخصص بطريقة منظمة. لكن عندما تتعرض هذه الآلات للتلف بفعل طفرات، يمكن أن ينقلب توازن نشاط الجينات باتجاه السرطان أو اضطرابات الدم أو مشكلات في تطور الدماغ. يشرح هذا المقال كيف يساعد فهم الأشكال ثلاثية الأبعاد لهذه الآلات العلماء على تحديد مكان الخلل وكيف يمكن إصلاحه.
عدة الخلايا لتعتيم الجينات
الميكروRNA عبارة عن قطع قصيرة من الحمض النووي الريبي، بطول نحو 22 وحدة بناء، لا تُشفِّر بروتينات بنفسها. بدلاً من ذلك، تلتصق بالرنا الرسول الأطول وتعلِّم إما بتدميره أو بمنع ترجمته، وبذلك تُخفّض نشاط الجين بدلاً من إيقافه تمامًا. لصنع هذه الميكروRNA، تمر الخلايا بسوابق ريبية أطول عبر خط تجميع مكوكي وممنهج. أولاً، يقتص إنزيم DROSHA المقطوعات الأولية الضخمة في نواة الخلية إلى قطع أقصر على شكل دثار شعرية. تنتقل هذه القطع بعد ذلك إلى السيتوبلازم، حيث يقيس إنزيم آخر، DICER، ويقصها إلى أزواج بحجم الميكروRNA. أخيرًا، تُحمَّل إحدى سلسلتي كل زوج في بروتين يُدعى أرغوناوت 2 (AGO2)، الذي يستخدم الميكروRNA كدليل للعثور على الرسائل المطابقة وكبتها. 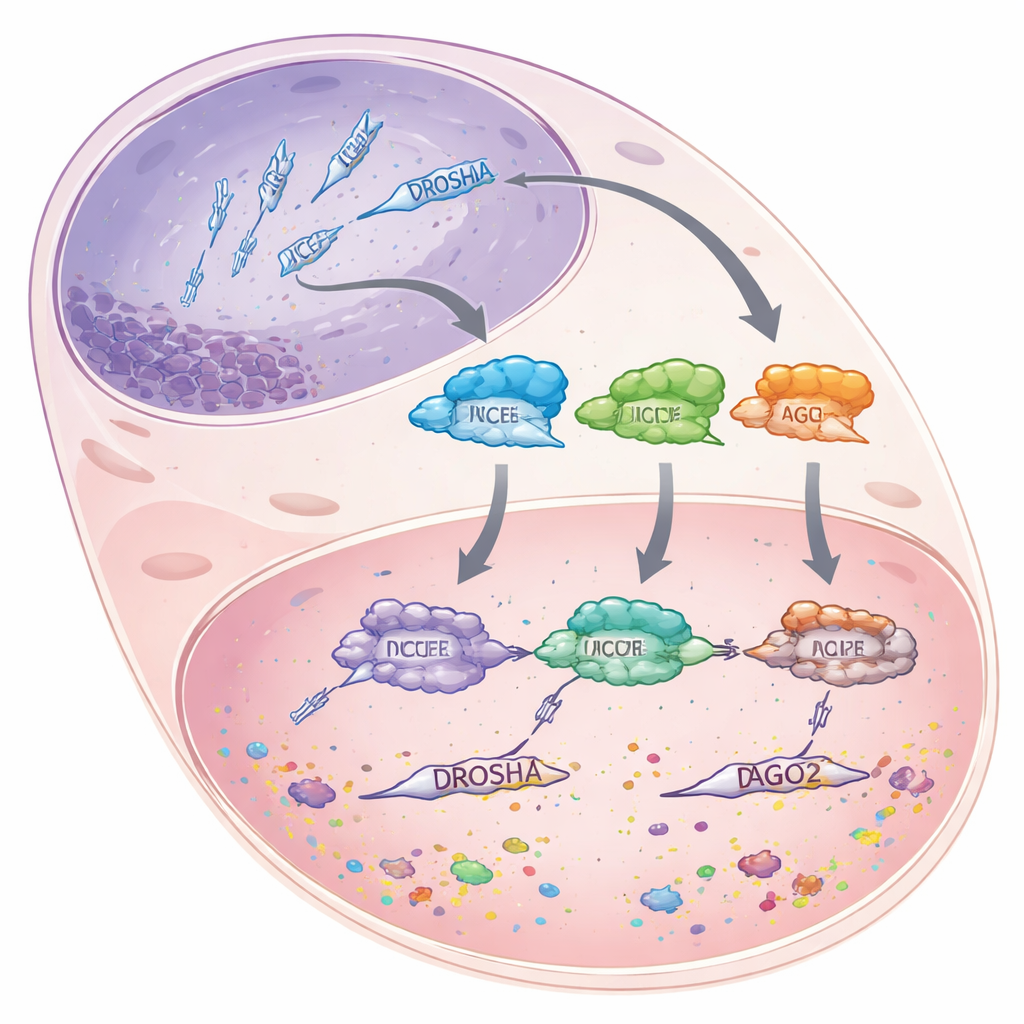
أشكال دقيقة لوظائف دقيقة
ليست DROSHA وDICER وAGO2 مقصات بسيطة؛ فكل منها مبني من أجزاء متفاعلة عدة يجب أن تتحرك بتنسيق راقص. تعمل DROSHA مع بروتين شريك، DGCR8، للإمساك بطرف دثار الميكروRNA الأولي وتحديد المكان الدقيق للقص. يستخدم DICER نوعًا من المسطرة المدمجة المتشكلة من نطاقاته لتعيين مسافة ثابتة بين مكان إمساكه لطرف الدثار ومركزه التحفيزي حيث يحدث القطع. يلتف AGO2 حول شريط ميكروRNA مفرد بحيث تُعرض منطقة «البذرة» فيه تمامًا للتعرف على الرسائل المستهدفة، بينما تصطف أيونات معدنية وحموض أمينية أساسية في قلبه لقص تلك الأهداف عندما يكون الاقتران قويًا بما فيه الكفاية. عبر البروتينات الثلاثة، توجه الأخاديد الموجبة الشحنة والروابط المرنة خيوط الرنا في مواضعها بينما تنفذ جيوب ربط المعادن والمخلفات التحفيزية القص الكيميائي.
عندما تنحرف أو تَفْقِد المقصات حدتها
كشفت دراسات جينية على مرضى السرطان واضطرابات الدم ومتلازمات التطور العصبي عن مجموعات من الطفرات في هذه «آلات» الميكروRNA. تقع العديد من التغييرات الأكثر ضررًا مباشرة في المراكز التحفيزية أو في أسطح القبض الضيقة على الرنا. في DROSHA، على سبيل المثال، تقع استبدالات مثل E1147K وD1219G في قلب موقع القطع وتعيق القدرة على احتجاز أيونات معدنية أساسية، مما يترك الإنزيم عاجزًا عن معالجة الميكروRNA الأولي. طفرات DROSHA أخرى، مثل الاختصارات التي تزيل منطقة القطع أو التغيرات التي تزعزع استقرار الدعامات اللولبية، تُضعف المركب بأكمله وتسبب انخفاضات شاملة في مستويات الميكروRNA في ورم ويلمز واضطرابات نقي العظم وأمراض الجهاز العصبي. في DICER، تتجمع طفرات متكررة في أحد نطاقي القطع لديها، مما يحرف الإنتاج بحيث يُفقد أحد ذراعي ثنائي الميكروRNA، وهو ما يغير التوازن بين الإشارات المروجة للنمو والمثبطة له. 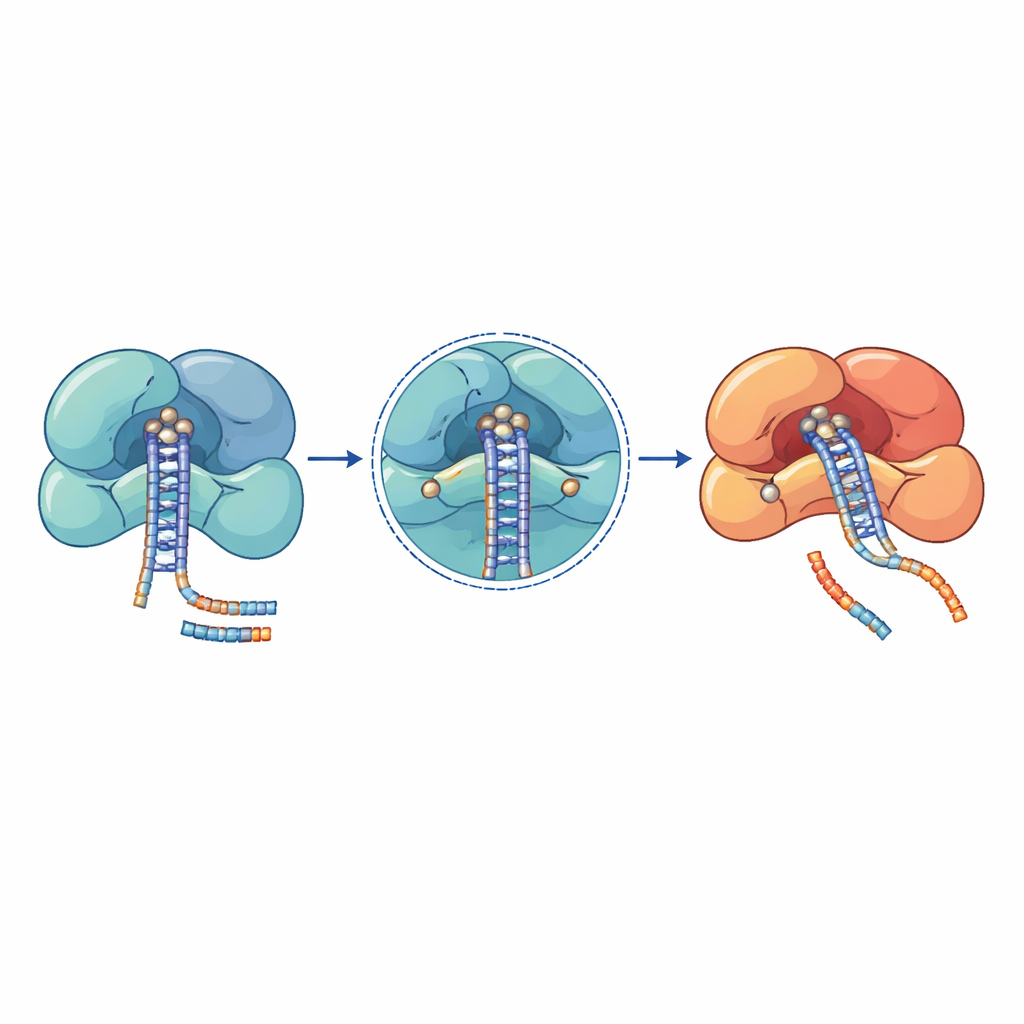
دلائل إرشاد غير مصطفة في الدماغ وخارجه
تحكي طفرات AGO2 قصة مختلفة لكنها ذات صلة. الضربات المباشرة إلى نواته التحفيزية نادرة، ربما لأنها ستكون قاتلة في مراحل مبكرة من التطور. بدلاً من ذلك، تميل المتغيرات المرتبطة بالمرض إلى الظهور في مناطق الروابط المرنة وعلى مفاصل النطاقات التي تحافظ على شكل AGO2. في متلازمة ليسل–كراينكامب، وهي حالة تطور عصبي، تُحدث طفرات في هذه الروابط والأسطح المحيطة بها التواءات دقيقة بطريقة حزم وحركة أجزاء PAZ وMID وPIWI في AGO2. يمكن أن يؤدي ذلك إلى محاذاة غير صحيحة للميكروRNA الدليلي أو إضعاف قبضة البروتين على الرنا المستهدف، مما يُبهم دقة كبح الجينات خلال تطور الدماغ. يمكن لتغييرات هيكلية مماثلة في أي نقطة على طول مسار الميكروRNA—سواء في DROSHA أو DICER أو AGO2—أن تمتد آثارها، وتغيّر شبكات كاملة من الجينات المشاركة في نمو الخلايا وتكوين الدم وتوصيل الخلايا العصبية.
تحويل الأدلة الهيكلية إلى علاجات مستقبلية
بإسقاط طفرات الأمراض على خرائط ثلاثية الأبعاد عالية الدقة لهذه البروتينات، يمكن للباحثين تصنيف كيفية تسبب كل تغيير بالمشكلة—سواء بتفتيح حد القطع، أو بإرخاء الاتصالات الحيوية مع البروتينات الشريكة، أو بثني الدعامات اللولبية الأساسية خارج المحاذاة. تفتح هذه الرؤى الهيكلية الباب أمام تدخلات مستهدفة: جزيئات صغيرة تُثبّت الواجهات الضعيفة، أو رنات مصممة تُعيد الإنزيمات ذات الوظيفة الجزئية إلى الركائز الصحيحة، أو مركبات كلوسيرية تدفع البروتينات المتحورة إلى أشكال أكثر نشاطًا. للمتابع غير المتخصص، الخلاصة أن التعديلات الهيكلية الضئيلة في مقصات الرنا الخلوية يمكن أن تُحدث تأثيرات كبيرة على الصحة، لكنها أيضًا توفّر مقابض دقيقة لتصميم علاجات من الجيل التالي تراعي الطفرات.
الاستشهاد: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
الكلمات المفتاحية: الميكروRNA, تداخل الحمض النووي الريبي, DROSHA DICER AGO2, وراثة السرطان, اضطرابات النمو العصبي