Clear Sky Science · ar
الآليات التنظيمية لاستقرار بروتين Snail: نظام اليوبكويتين–بروتيزوم والتحلل التلقائي الوسيط بوساطة الجزيئات المرافقة
لماذا انتشار السرطان يعتمد على بروتين هش
تصبح سريرية السرطان مهددة للحياة حقًا عندما تنفصل الخلايا عن الورم الأصلي وتنتقل إلى أعضاء بعيدة. هذا الانتشار، أو الانتقال النقيلي، يعتمد جزئيًا على بروتين «المفتاح الرئيسي» القوي المسمى Snail، الذي يساعد الخلايا على تفكيك وصلاتها لتصبح أكثر قدرة على الحركة. تشرح هذه المقالة كيف تحافظ خلايانا عادةً على تحكم صارم في مستوى Snail عبر تفكيكه السريع بواسطة نظامي تصريف رئيسيين للفضلات. فهم هذا التوازن يفتح آفاقًا جديدة لإبطاء أو منع الانتقال النقيلي.
من خلايا مضغوطة إلى غزاة متجولين
في الأنسجة الصحية، تُشكّل الخلايا الطلائية طبقات مرتبة تشبه الطوب تبقى في أماكنها وتتلاصق بإحكام مع جيرانها. لكي تهرب خلية ورمية، غالبًا ما تمر بتحول يُسمى التحول الطلائي–الوسِيطي (EMT)، تفقد خلاله اتصالاتها الضيقة وتكتسب قدرة على الحركة والغزو. يُعد Snail محركًا رئيسيًا لهذا التحول: عندما يتواجد داخل نواة الخلية، يطفئ جينات تحافظ على التصاق الخلايا ببعضها ويشغّل جينات تُعزّز الحركة والغزو. ترتبط المستويات العالية من Snail بسرطانات عدوانية وبنتائج سلبية للمرضى، لذا طورت الخلايا طرقًا للحفاظ على ندرة Snail وقصر عمره في الظروف العادية.
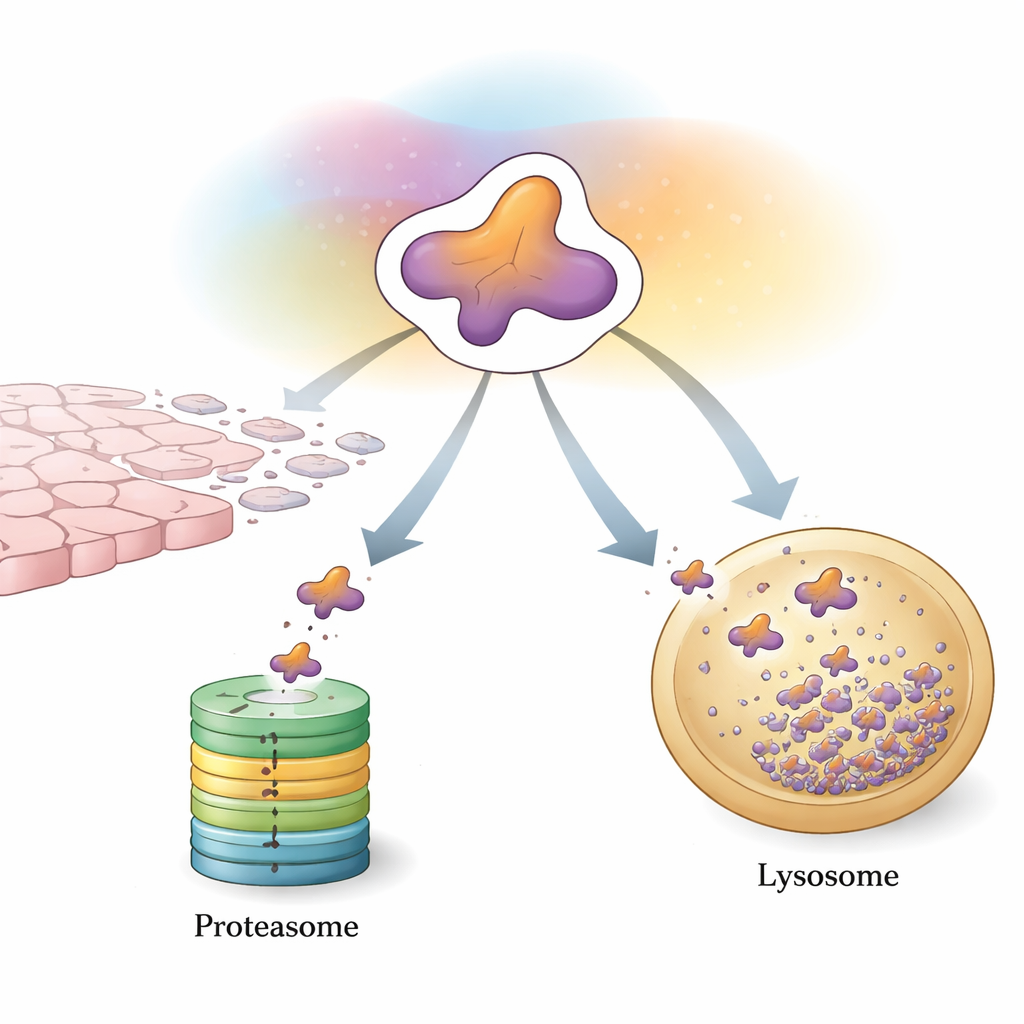
الخط الأول للسيطرة داخل الخلية: تعليم وتمزيق
إحدى الطرق الرئيسية التي تتحكم بها الخلايا في Snail هي نظام اليوبكويتين–بروتيزوم، آلة تعليم وتمزيق للبروتينات غير المرغوب فيها. تقوم إنزيمات متخصصة بإلحاق «أعلام» صغيرة مصنوعة من بروتين يُدعى اليوبكويتين إلى Snail. عندما تتراكم هذه الأعلام بنمط معين، يتم توجيه Snail إلى البروتيزوم، وهو مركب يشبه البرميل يقوم بتقسيمه إلى قطع. مجموعة كبيرة من البروتينات المساعدة تضبط هذه العملية بدقة. بعض الإنزيمات تضع سلاسل تحفّز التحلل التي ترسل Snail بسرعة إلى المفرمة، مما يساعد على تقييد نمو الورم وانتشاره. أما أخرى فتضيف سلاسل تُثبّت Snail أو تعزز إنتاجه الجيني بشكل غير مباشر، مما يميل بالتوازن نحو EMT والانتقال النقيلي. التعديلات الكيميائية مثل الفسفرة والأستلة تعمل كمفاتيح إضافية، تتحكم في أي المساعدين يمكنهم الارتباط بـSnail وما إذا كان سيُدمر أم يُرحّم.
رفع الكوابح: إنزيمات تنقذ Snail
القصة لا تنتهي بوضع العلم على Snail فحسب. هناك مجموعة أخرى من الإنزيمات، تُسمى نزع اليوبكويتين، قادرة على نزع أعلام اليوبكويتين، مخلّصة بذلك Snail من البروتيزوم. يُفعّل العديد من هذه الإنزيمات أو يُقوّى في السرطانات، مما يسمح لـSnail بالتهرب من التحلل والاستمرار في النواة. تعتمد أفعالها بشكل كبير على السياق الخلوي: في بعض الحالات تثبت Snail مباشرة، وفي حالات أخرى تؤثر على موضع Snail داخل الخلية أو كيفية تفاعله مع البروتينات الشريكة. تصل إشارات من مسارات مرتبطة بالسرطان، مثل عوامل النمو واستجابات الإجهاد، إلى هذه الشبكة، لتقرر ما إذا كان سيتم إزالة Snail بسرعة أو السماح له بتشغيل برنامج EMT.
شبكة أمان ثانية: توصيل انتقائي إلى مركز إعادة التدوير داخل الخلية
بعيدًا عن البروتيزوم، تعتمد الخلايا على الالتهام الذاتي، مجموعة من المسارات التي تنقل البروتينات إلى مقصورات حمضية تُدعى الجسيمات الحالة (الليسوزومات) لتفككها. تُبرز هذه المراجعة شكلاً انتقائيًا عالي الاختيار يعرف بالالتهام الذاتي الوسيط بالمساعدات (CMA) كطريق رئيسي ثانٍ للتحكم في Snail. يتعرف CMA على تسلسل قصير داخل Snail، وبمساعدة بروتينات مرافقة، يسلم Snail الخلوي إلى الجسيمات الحالة لتدميره. في خلايا سرطان الثدي الأقل عدوانية، يحافظ هذا النظام على Snail إلى حد كبير خارج النواة ومعرضًا للإزالة الليزوزومية. في سرطانات الثدي الثلاثية السلبية الأكثر عدوانية، يميل Snail إلى التراكم في النواة وتفادي CMA، مما يعزز قدرته على تحفيز EMT والانتقال النقيلي.
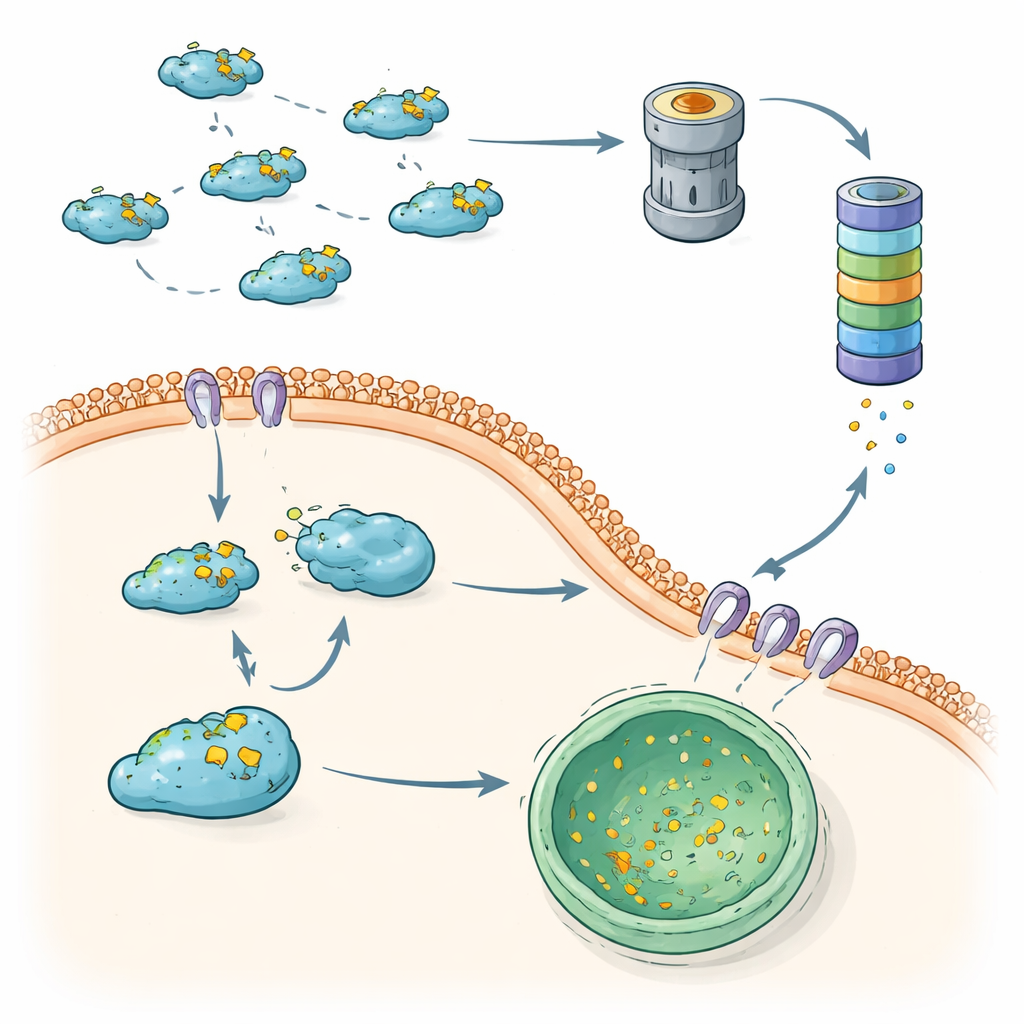
عندما يفشل ضبط الجودة، يزداد الانتقال النقيلي
تُظهر هذه النتائج مجتمعة أن الخلايا تستخدم محورين تكميليين لـ"ضبط الجودة" لكبح Snail: مسار اليوبكويتين–بروتيزوم والتحلل الليزوزومي القائم على CMA. عندما يعمل كلاهما بشكل صحيح، يُستبدل Snail بسرعة، مما يحدّ من EMT ويساعد على منع خلايا الورم من الانتشار. عندما يضعف أي محور—من خلال تغيّرات في إنزيمات التعليم، أو نازعي اليوبكويتين، أو مكونات CMA—يصبح Snail أكثر استقرارًا، ويتراكم في النواة، ويعزّز سلوكًا اقتحاميًا قويًا. من خلال رسم خريطة لهذه المسارات المتصلة لتحلل البروتين، تطرح المقالة إمكانيات علاجية جديدة: أدوية تعيد أو تعزز تحلل Snail، أو توجه Snail مرة أخرى نحو CMA أو التحلل البروتيزومي، قد تساعد في إعادة تطبيق الكوابح على الانتقال النقيلي من دون إيقاف هذه الأنظمة الأساسية لإعادة تدوير البروتين تمامًا.
الاستشهاد: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
الكلمات المفتاحية: نقائل السرطان, التحول البِيامِقِطِري–الوسِيطِي (الظهاري–اللحمي), بروتين Snail, تحلل البروتين, الالتهام الذاتي