Clear Sky Science · ar
تقدّم التصلّب المتعدد المرتبط بالميكروجليا: تحديد الأهداف والتعامل العلاجي في نماذج بشرية مختبرية
لماذا تهم خلايا المناعة الدماغية في التصلب المتعدد
يوصف التصلّب المتعدد (MS) غالبًا بأنه مرض يهاجم فيه جهاز المناعة الجسم — وبشكل خاص الدماغ والنخاع الشوكي. العديد من الأدوية الحالية تقلل بنجاح من النوبات المفاجئة، أو الانتكاسات، لكنها لا توقف التدهور البطيء والصامت الذي يعاني منه كثير من المرضى على مدى سنوات. تشرح هذه المراجعة كيف أن خلايا مناعية صغيرة تعيش بشكل دائم في الدماغ، تُدعى الميكروجليا، قد تكون محركًا لذلك التراجع طويل الأمد — وكيف أن نماذج دماغ بشرية مزروعة في المختبر تساعد العلماء في العثور على علاجات يمكنها أخيرًا إبطاء أو إيقاف التقدّم.
المحرّك الخفي للضرر المستمر
تقسّم التصلّب المتعدد تقليديًا إلى أشكال نكسية وتقدّمية، لكن الأدلة تُظهر الآن أن التقدّم يبدأ مبكرًا جدًا لدى نحو الجميع المصابين، حتى عندما يبدون في المظهر وكأنهم يعانون نكسات فقط. بينما تغذّي النكسات خلايا مناعية تدخل من الدم، يبدو أن التقدّم مدفوع بالتهاب محاصر داخل الدماغ والنخاع الشوكي. في هذا المحيط المُغلق، تشارك الميكروجليا في العديد من العمليات الضارة: التهاب مستمر، فقدان الغمد المياليني العازل للألياف العصبية في المادة البيضاء والرمادية، تراكم مركبات مؤكسِدة ضارة، وفشل في عمليات الإصلاح. النتيجة النهائية هي الفقدان التدريجي للخلايا العصبية وتوصيلاتها. عادةً ما تساعد الميكروجليا في الحفاظ على صحة الدماغ عن طريق إزالة الحطام ودعم الخلايا العصبية، لكن في التصلّب المتعدد تتحول غالبًا إلى حالات أكثر عدائية وتفقد بعض أدوارها الوقائية، مما يجعلها مشتبهًا بها رئيسيًا في دفع التقدّم.
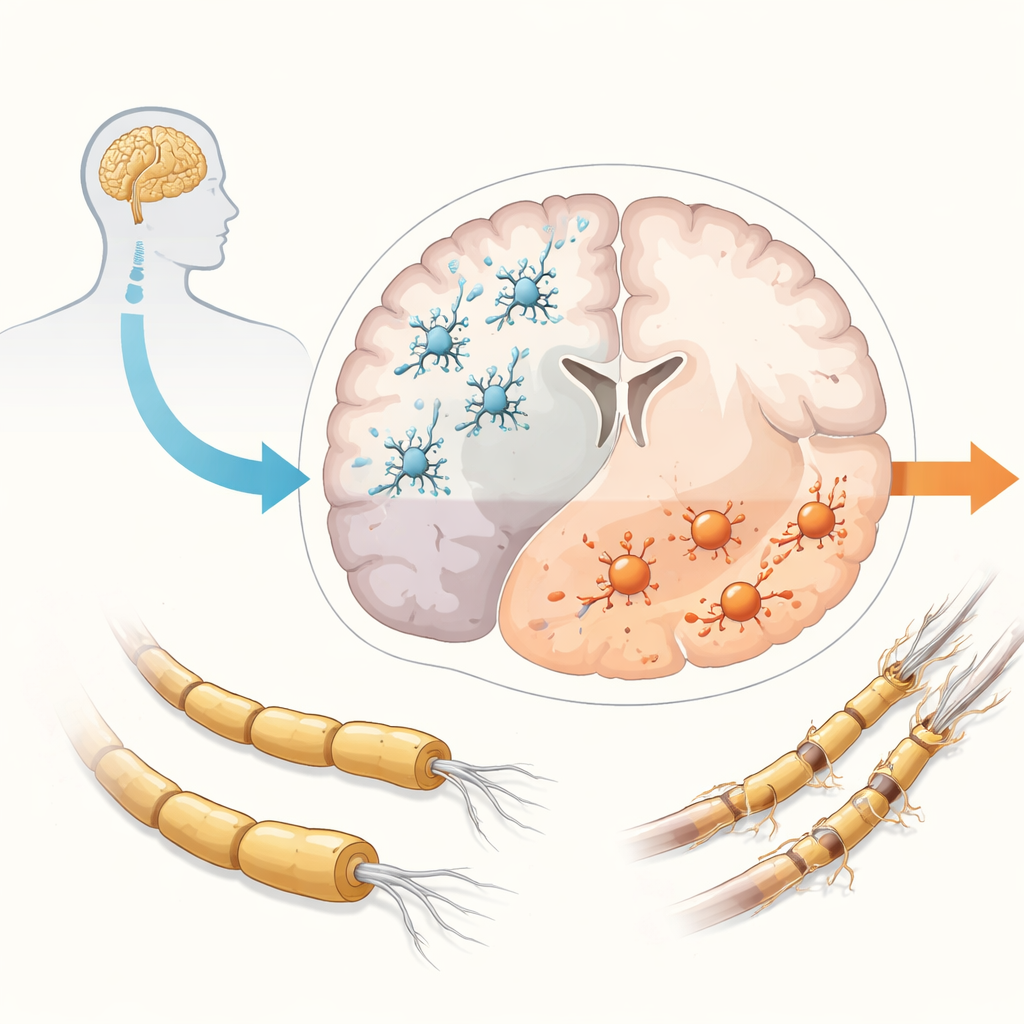
لماذا تقصُر نماذج الحيوانات التقليدية
على مدار عقود، كانت الدراسات في الفئران وغيرها من الحيوانات حاسمة في تطوير أدوية تحدّ من النكسات، لكنها فشلت إلى حد كبير في إنتاج علاجات توقف التقدّم. أحد الأسباب أن نماذج الحيوانات تحاكي التصلّب المتعدد البشري جزئيًا فقط ولا تعيد بدقة الالتهاب المعقّد والمستديم الذي يظهر في أدمغة المرضى. كما تختلف ميكروجليا القوارض عن الميكروجليا البشرية في جينات واستجابات مهمة. كنتيجة لذلك، العلاجات التي تبدو واعدة في الحيوانات غالبًا لا تجدي نفعًا لدى البشر. أدّى نقص نماذج حيوانية تلتقط حقًا التصلّب المتقدم إلى دفع الباحثين لبناء أنظمة بشرية جديدة في المختبر، حيث يمكنهم دراسة الميكروجليا وخلايا الدماغ الأخرى بصورة أكثر مباشرة.
بناء نماذج دماغ بشرية في أطباق
يستخدم العلماء الآن عدة مستويات من النماذج المختبرية لدراسة الميكروجليا البشرية. الخلايا الأولية المأخوذة مباشرة من نسيج دماغي من القوارض أو البشر تحافظ على العديد من الصفات الطبيعية لكنها صعبة الحصول، وتتغير بسرعة خارج بيئتها الأصلية، ولا يمكن توسيعها بسهولة بكميات كبيرة. للتغلب على هذه العقبات، يلجأ الباحثون إلى الخلايا الجذعية المستحثة متعددة القدرات (iPS) — خلايا بالغة أعيد برمجتها إلى حالة جذعية مرنة. يمكن توجيه هذه الخلايا لتتحول إلى ميكروجليا أو نيورونات أو خلايا دماغية أخرى. في المزارع المسطحة البسيطة، تلتقط ميكروجليا المشتقة من iPS العديد من السمات الرئيسية ويمكن إنتاجها بأعداد كبيرة، مما يتيح تجارب مفصّلة وشاشات للأدوية. ويمكن حتى إنتاجها من مرضى مصابين بالتصلّب المتعدد، كاشفة فروقًا داخلية مثل تغيّر نشاط الجينات وتبدلات في كيفية استجابة هذه الخلايا للإجهاد وإزالة الحطام.
إضافة بيئات دماغية أكثر واقعية
بما أن سلوك الميكروجليا يتشكّل بقوة حسب محيطه، انتقل الباحثون إلى ما يتجاوز طبقات الخلايا المفردة إلى ترتيبات أكثر واقعية. في المزارع ثنائية الأبعاد المشتركة، تنمو الميكروجليا مع النيورونات والخلايا الداعمة، ما يساعدها على تبنّي أشكال وسلوكيات أكثر طبيعية ويتيح للعلماء فحص كيفية تأثير أنواع الخلايا على بعضها البعض. الكريات ثلاثية الأبعاد والأورجانويدات — قطع صغيرة ذاتية التنظيم من نسيج شبيه بالدماغ — تذهب أبعد من ذلك، فتوفّر بيئة طرية ومزدحمة تشبه نسيج الدماغ الفعلي بشكل أوثق. عندما تُدمج الميكروجليا في هذه البُنى، تُظهر أشكال تفرعية معقدة، وتستجيب للضرر، وتتفاعل مع طبقة شبيهة بالحاجز الدماغي الوعائي، وتستجيب لإشارات التهاب من سائل النخاع للمرضى المصابين بالتصلّب المتعدد. استُخدمت مثل هذه النماذج لدراسة كيف يثير الالتهاب المزمن حالة «متعبة لكنها ملتهبة» تُعرف بالهرم الخلوي لدى الميكروجليا والخلايا النجمية، وكيف أن تغيّرات في معالجة الدهون لدى الميكروجليا قد تضعف إصلاح المايلين. وبالموازاة، يسمح زرع ميكروجليا بشرية مشتقة من iPS أو أورجانويدات في أدمغة الفئران لهذه الخلايا بالنضج أكثر داخل شبكة حية وليتم اختبارها في نماذج مرضية شبيهة بالتصلّب المتعدد القائمة مسبقًا.
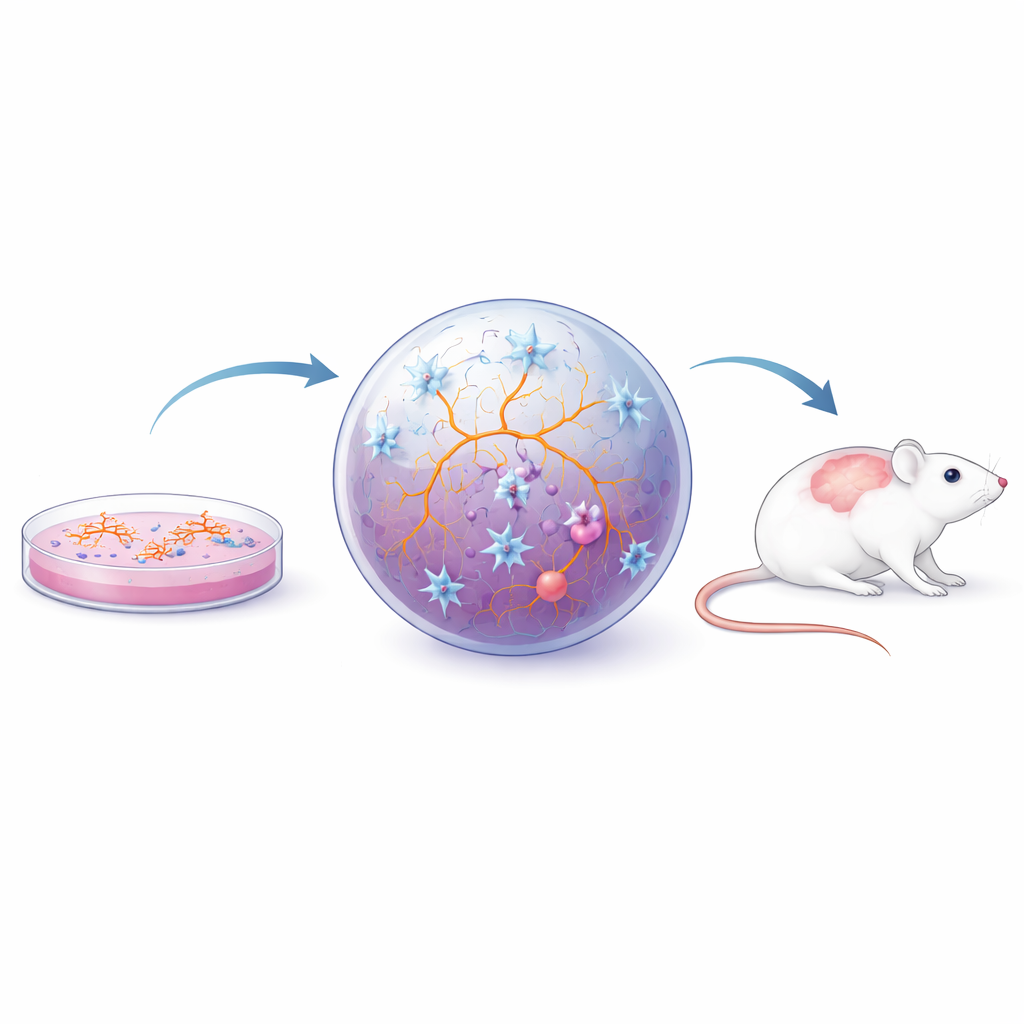
من نماذج المختبر إلى علاجات مستقبلية
تشكّل هذه النماذج البشرية المختبرية والمهجنة معًا صندوق أدوات لتحليل كيفية مساهمة الميكروجليا في تقدّم التصلّب المتعدد وللاختبار التجريبي لعلاجات جديدة تهدف إلى تهدئة النشاط الميكروجليائي الضار مع استعادة وظائفه الوقائية. وعلى الرغم من أن أيًا من هذه النماذج لا يعيد كامل الدماغ البشري، فإن كل نموذج يلتقط قطعًا مختلفة من اللغز، ومعًا يجسرون الهوة بين زراعة الخلايا البسيطة والنماذج الحيوانية غير الكاملة. من خلال الجمع بين الرؤى المستخلصة من هذه الأنظمة، يأمل الباحثون في تحديد أهداف دوائية دقيقة — مثل المسارات التي تتحكم في الالتهاب، وتغيرات شبيهة بالشيخوخة، واستقلاب الدهون في الميكروجليا — والتي قد تترجم أخيرًا إلى علاجات تبطئ أو توقف العجز التدريجي الذي يميّز التصلّب المتعدد التقدّمي.
الاستشهاد: Blenkle, A., Geladaris, A. & Weber, M.S. Microglia-associated progression of multiple sclerosis: target identification and therapeutic engagement in human in vitro models. Exp Mol Med 58, 357–365 (2026). https://doi.org/10.1038/s12276-026-01647-w
الكلمات المفتاحية: تقدّم التصلب المتعدد, الميكروجليا, خلايا جذعية مستحثة متعددة القدرات, أورجانويدات دماغية, الالتهاب العصبي