Clear Sky Science · ar
البروتين الحساس للأكسدة HMGB1: أدواره داخل الخلية وخارجها
لماذا يهم بروتين يتغير شكله للصحة
داخل كل خلية تقريبًا في جسمك يوجد بروتين صغير يُدعى HMGB1 يتصرف قليلاً مثل أداة متعددة الاستخدامات. في الظروف الهادئة يساعد بهدوء في تنظيم الحمض النووي. لكن عندما تتعرض الخلايا للإجهاد أو التلف، يمكن أن يخرج HMGB1 من النواة، وينزلق إلى الأنسجة المحيطة، ويعمل كإشارة إنذار للجهاز المناعي. تستعرض هذه المقالة المراجعية كيف تحوّل تغييرات كيميائية دقيقة مدفوعة بالأكسدة HMGB1 إلى شخصيات بيولوجية مختلفة تمامًا — بعضها يحمي الأنسجة، وبعضها يدفع الالتهاب، وبعضها قد يساهم في الأمراض المزمنة. فهم "خاتم المزاج" الجزيئي هذا قد يفتح سبلًا جديدة لتهدئة الالتهاب المفرط دون إيقاف الجهاز المناعي تمامًا.
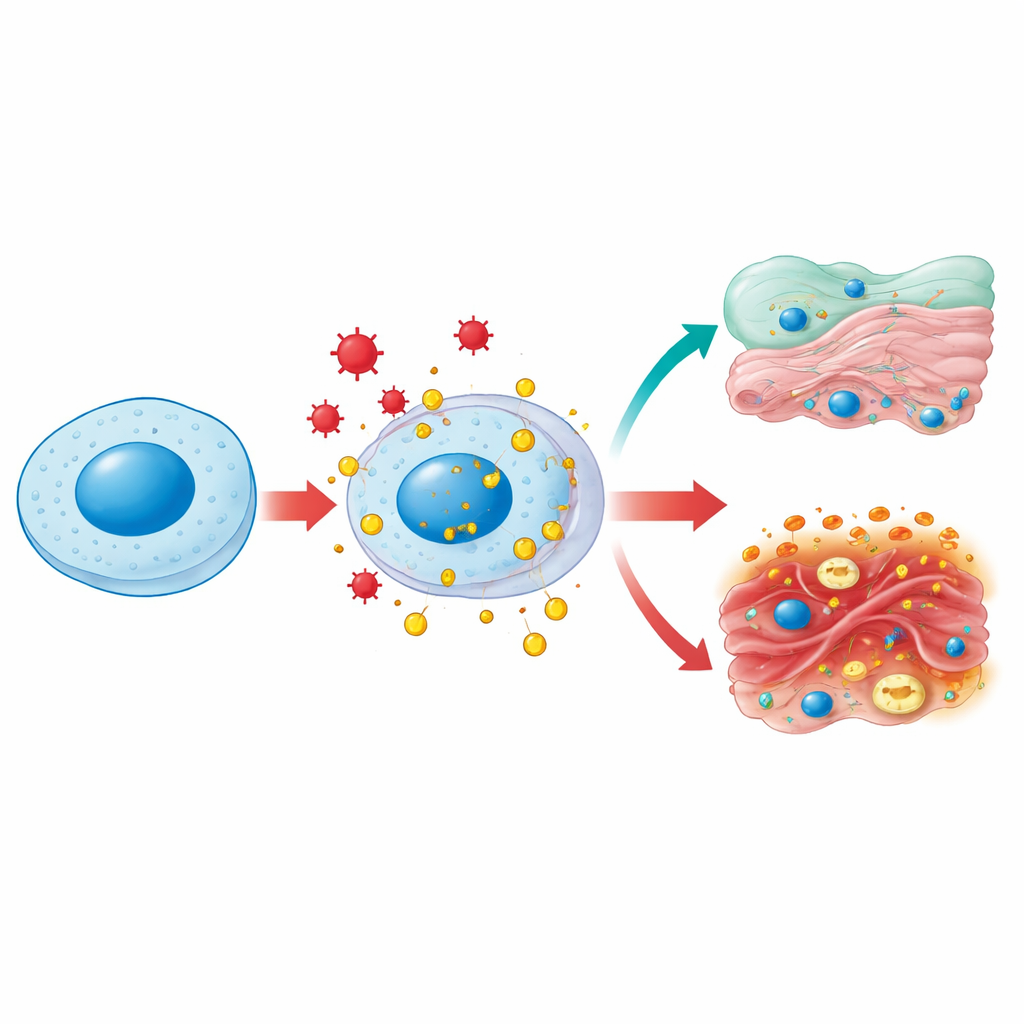
بروتين واحد، أدوار متعددة
يعيش HMGB1 عادة في نواة الخلية، حيث يثني ويرخِّي الحمض النووي لتسهيل نسخ الجينات وإصلاحها. تحت الإجهاد — مثل العدوى، ارتفاع سكر الدم، أو الإصابة السامة — يمكن أن يتعرض لتعديلات كيميائية ويُرافق خارجًا إلى داخل الخلية المائي ثم إلى العالم الخارجي. في السيتوبلازم يساعد HMGB1 في الحفاظ على صحة الميتوكوندريا، مصانع طاقة الخلية، عن طريق تشجيع عملية التنظيف الذاتية المسماة التحلل الذاتي (autophagy) ومنع تفكك هذه العضيات بشكل مفرط. عند إفرازه خارج الخلية، يصبح HMGB1 إشارة "خطر" كلاسيكية: تتعرف الخلايا المناعية عليه كدليل على إصابة الأنسجة وتهرع إلى موقع الضرر. لذا يلعب نفس الجزيء أدوارًا منزلية داخل الخلايا وأدوار إطلاق إنذار خارجها، اعتمادًا على مكانه وكيفية ضبطه كيميائيًا.
كيف تعيد الأكسدة كتابة سلوكه
المحور المركزي لهذه المراجعة هو كيف تعيد الأكسدة — التفاعلات المدفوعة بجذور الأكسجين التفاعلية (ROS) — تشكيل HMGB1. يحتوي البروتين على ثلاث وحدات تحمل الكبريت تعمل كمفاتيح صغيرة. في حالتها المختزلة بالكامل، يميل HMGB1 إلى دعم بقاء الخلايا وجذب خلايا الإصلاح. يمكن للأكسدة الخفيفة أن تربط اثنين من هذه المواقع معًا داخل نفس البروتين، مكونة شكلًا "ثنائي الكبريتيد" يكون جيدًا بشكل خاص في الالتصاق بمستقبلات مناعية مثل مستقبلات شبيهة Toll وRAGE على أسطح الخلايا. هذا الشكل يحفز إنتاج الرسل الالتهابية بشدة. يمكن للإجهاد التأكسدي الأقوى أن يدفع الجزيء إلى شكل مفرط الأكسدة لا يعود قادرًا على الارتباط بالحمض النووي أو بالمستقبلات بفعالية؛ يصبح هذا الشكل "المحترق" صامتًا مناعيًا ويرتبط بمرحلة حل الالتهاب وبرامج موت الخلايا التي لا تثير هجومًا مناعيًا.
من إشارات موت الخلايا إلى محركات المرض
يرتبط HMGB1 ارتباطًا عميقًا بطرق موت الخلايا المتعددة. أثناء أشكال الموت العنيفة مثل النخر (necrosis)، النخر المبرمج (necroptosis)، الفيروبتوسيس (ferroptosis)، والبايروبتوسيس (pyroptosis)، يتسرب HMGB1 أو يُنقل بنشاط خارج الخلايا حاملاً بصمة تأكسدية تعكس ظروف الأكسدة المحيطة. في المراحل المبكرة من النخر يميل إلى أن يكون في شكل مختزل، بينما يدفع الإجهاد المطول تجاه حالات أكثر أكسدة. بمجرد خروجه، يمكن للـ HMGB1 المختزل أن يعزز التحلل الذاتي الوقائي في بعض خلايا السرطان، مما يساعدها على النجاة من العلاج الكيميائي، بينما تضخم الأشكال الغنية بالثنائيات الكبريتية والأشكال المزدوجة الشلالات الالتهابية وتنشيط النظام التكميلي الذي قد يفاقم تلف الأنسجة. يمكن أن يعيد HMGB1 أيضًا تغذية نفسه لتعزيز مسارات موت معينة — على سبيل المثال من خلال الشراكة مع دهون بكتيرية لتحفيز النخر المبرمج أو عن طريق دفع موت الخلايا المعتمد على الحديد في خلايا الدعم الدماغية بعد السكتة الدماغية. بهذه الطريقة، يؤشر HMGB1 ويعدّل توازن الحياة والموت في الأنسجة.
روابط بالالتهاب والمناعة الذاتية والسرطان
لأن سلوكه حساس جدًا للأكسدة، تظهر متغيرات HMGB1 بأنماط مميزة عبر الأمراض. يرتبط HMGB1 الغني بالثنائيات الكبريتية ارتباطًا قويًا بالالتهاب المزمن: يظهر في المفاصل الملتهبة في التهاب المفاصل الروماتويدي، في تليف الكبد، في إصابة الرئة، في تلف الإقفار–إعادة التروية بعد الجراحة، وفي الإنتان، حيث تتوافق مستويات الدم معه ومع شدة المرض ومخاطر الوفاة. بالمقابل غالبًا ما يرافق HMGB1 المختزل حركة الخلايا وإعادة تشكيل الأنسجة، مثل تحرك الليف القلبي أو الخلايا الوحيدة الموجهة بواسطة الكيموكين CXCL12. يكون HMGB1 المفرط الأكسدة الصامت مناعيًا غنيًا في حالات مثل المراحل المتأخرة للموت المبرمج (apoptosis)، حيث يرغب الجسم في إزالة الخلايا المحتضرة دون إثارة هجوم. في الأورام، يدعم الشكل الثنائي الكبريت بيئة مناعية كابحة ومواتية للنمو، بينما يمكن أن يؤدي حجب HMGB1 إلى تقلص الأورام وجعل علاجات نقط التفتيش المناعية أكثر فعالية.
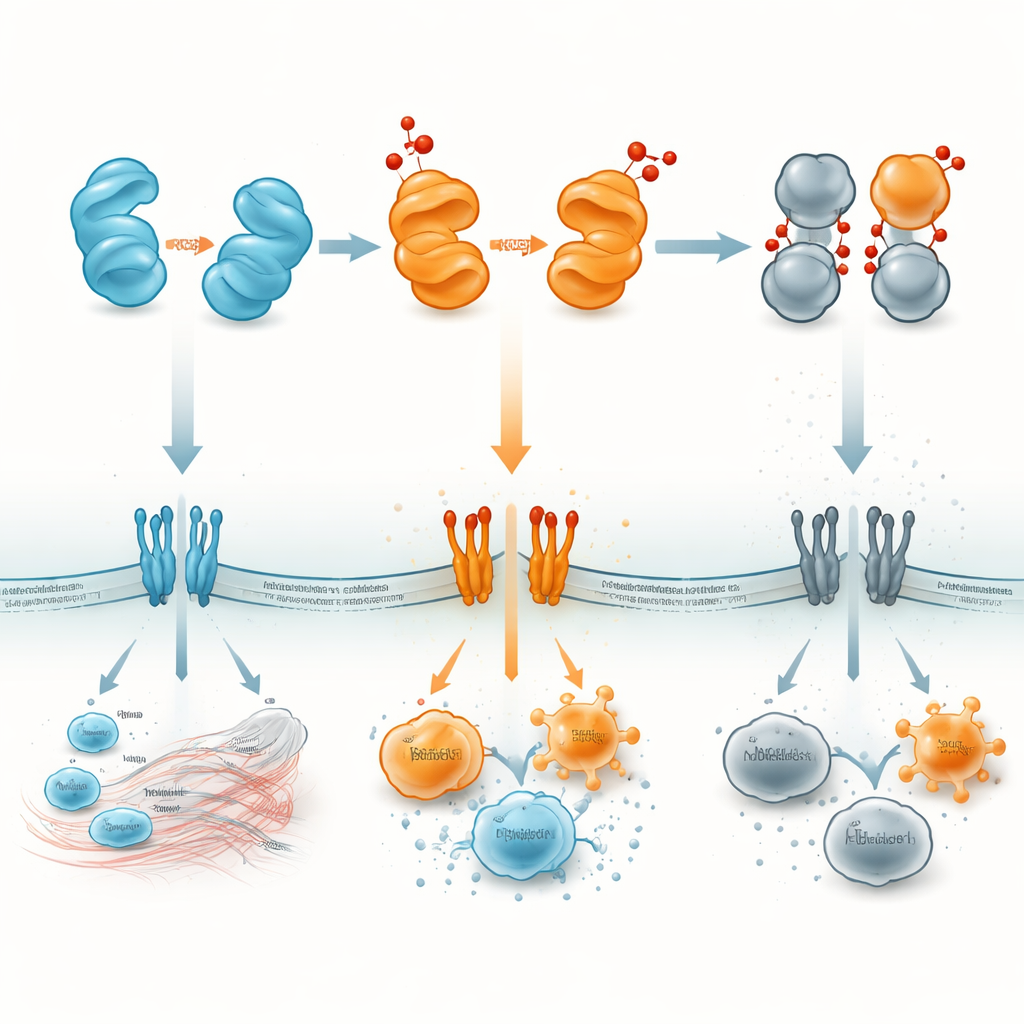
تحويل إنذار جزيئي إلى هدف علاجي
للمراقب العادي، يمكن التفكير في HMGB1 كجهاز إنذار جزيئي صغير يتغير مستوى صوته ورسالتُه مع حالته الكيميائية. يميل HMGB1 المختزل إلى استدعاء طواقم الإصلاح؛ الأشكال الثنائية والمزدوجة يمكن أن تصدر إنذارًا صارخًا يُغذي التهابًا ضارًا؛ والشكل المؤكسد بالكامل يخبِت عمليًا، مساعدًا على إنهاء الالتهاب. من خلال رسم خرائط أين ومتى يظهر كل شكل — داخل الأنوية، في السيتوبلازم، في الدم، أو في أعضاء محددة — يأمل الباحثون في تصميم أدوية تحجب الأشكال الضارة أو تُثبّت الأشكال المفيدة. قد تسمح مثل هذه الاستراتيجيات للأطباء بعلاج الإنتان، أمراض المناعة الذاتية، السكتة الدماغية، إصابة الرئة، أو السرطان عن طريق استهداف ليس HMGB1 نفسه فحسب، بل "مفتاح التقليل التأكسدي" الذي يتحكم في كيفية تواصل هذا البروتين مع الجهاز المناعي.
الاستشهاد: Kwak, M.S., Jung, S.F., Park, I.H. et al. The redox-sensitive protein HMGB1: intracellular and extracellular roles. Exp Mol Med 58, 345–356 (2026). https://doi.org/10.1038/s12276-026-01640-3
الكلمات المفتاحية: HMGB1, الالتهاب, الإجهاد التأكسدي, موت الخلايا, أمراض المناعة الذاتية