Clear Sky Science · ar
UBE2M كجسر يربط بين التأشير بالنِدّ (neddylation) وتنظيم دورة الخلية في سرطان الغدد القولونية المستقيمية
لماذا تهم هذه الدراسة لسرطان الأمعاء
يعد سرطان القولون والمستقيم من أكثر السرطانات شيوعًا وفتكًا في العالم، ويرجع جزء كبير من ذلك إلى قدرة خلايا الورم على الانقسام بلا هوادة. تكشف هذه الدراسة عن مفتاح تحكّم مخفي يساعد خلايا سرطان القولون والمستقيم على المرور بسرعة عبر نقطة تفتيش حاسمة في انقسام الخلية. من خلال توضيح كيفية عمل هذا المفتاح على المستوى الجزيئي — وإظهار أن دواء مضاد للفطريات موجود بالفعل يمكن أن يتداخل معه — تشير النتائج إلى طريقة محتملة جديدة لإبطاء أو وقف نمو الورم.
طبقة تحكم مخفية داخل خلايا الورم
الخلايا لا تنقسم عشوائيًا؛ بل تمر بدورة منظمة تحتوي على نقاط تفتيش تؤكد ما إذا كان من الآمن نسخ الحمض النووي والانقسام إلى خليتين. غالبًا ما تتلاعب الخلايا السرطانية بهذه النقاط. ركز الباحثون على عملية وسم كيميائية تُسمى التأشير بالنِدّ (neddylation)، التي تُعدّل البروتينات بعد تصنيعها بشكل دقيق. أشارت دراسات سابقة إلى أن نشاط التأشير بالنِدّ أعلى في العديد من السرطانات، لكن الرابط بينه وبين دورة الانقسام في خلايا سرطان القولون والمستقيم لم يكن واضحًا. باستخدام مجموعات بيانات كبيرة على مستوى الخلية المفردة من أورام بشرية، إلى جانب بيانات التعبير الجيني الإجمالية لأكثر من 1800 مريض، وجد الفريق أن نشاط التأشير بالنِدّ مرتفع بشكل خاص في الخلايا الخبيثة في مرحلة G2/M — البوابة النهائية قبل انقسام الخلية.
تسليط الضوء على بروتين "جسر" جزيئي
لاستخلاص الجزيئات التي تربط التأشير بالنِدّ بانقسام الخلايا، استخدم الباحثون تحليلات حسابية شبيهة بالشبكات لتصفية آلاف الجينات. برز بروتين واحد: UBE2M، إنزيم يساعد على إرفاق وسم NEDD8 الصغير بالبروتينات الأخرى. لم يرتبط UBE2M بقوة بمسارات التأشير بالنِدّ ودورة الخلية في البيانات فحسب؛ بل وُجد أيضًا بمستويات أعلى بكثير في أورام القولون مقارنة بالنسيج الطبيعي المجاور. يميل مرضى الأورام التي تحتوي كميات أكبر من UBE2M إلى نتائج بقاء أسوأ، مما يشير إلى أنه قد يكون محركًا للمرض وليس مجرد مرافقة. عندما قلّل الفريق من UBE2M في خطوط خلايا سرطانية ونماذج أورام في الفئران، تباطأ نمو الورم، وقلّت الانقسامات الخلوية، وزاد معدل موت الخلايا المبرمج. بالمقابل، أدى إجبار الخلايا على إنتاج كميات إضافية من UBE2M إلى تسريع النمو وتقدم دورة الخلية.
تتابع يحمي بروتينًا رئيسيًا محفزًا للنمو
بالغوص أعمق، سأل العلماء كيف يساعد UBE2M الخلايا على الانقسام. اكتشفوا أن UBE2M لا يعمل وحده بل يُشغّل تتابعًا يشمل بروتينين آخرين، USP39 وPABPC1. عادةً ما تُوسَم PABPC1 بسلاسل من علامات اليوبكويتين التي توجهها إلى آلية إعادة تدوير البروتينات في الخلية. أظهر الفريق أن UBE2M يعدّل كيميائيًا USP39 بوَسْم NEDD8. يعزز هذا الوَسْم قدرة USP39 على قطع سلاسل اليوبكويتين عن PABPC1، ما ينقذها من التحلل ويجعلها أكثر استقرارًا. بوجود مزيد من PABPC1، تصبح الخلية أفضل في ترجمة رسائل رنا المرسال المحددة إلى بروتين، بما في ذلك الرنا المرسال الخاص بـ CCNB1، وهو سيكلين يعمل كدواسة تسريع لنقطة تفتيش G2/M. بعبارة أخرى، يساعد UBE2M على استقرار PABPC1، والذي بدوره يعزز إنتاج CCNB1، دافعًا الخلايا نحو الانقسام بسهولة أكبر.
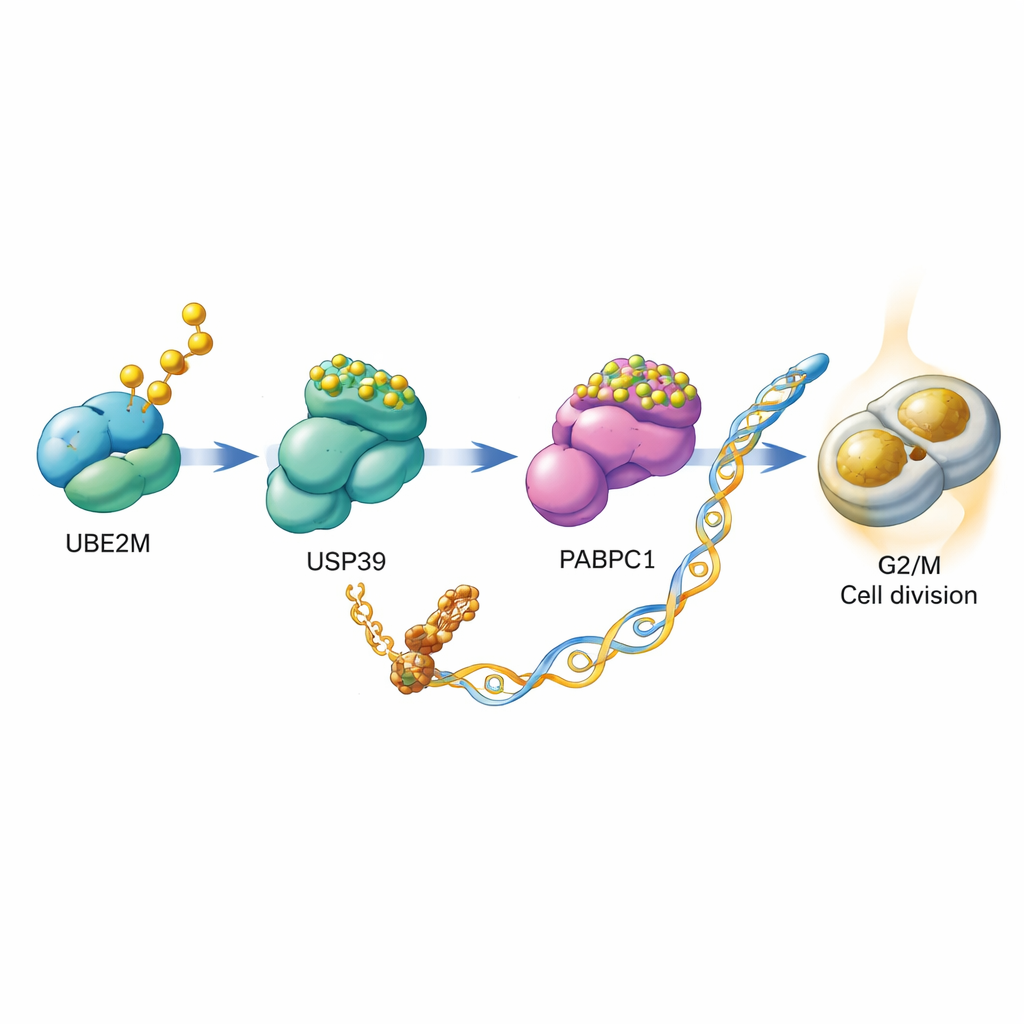
من الآلية الجزيئية إلى فرصة دوائية
أشارت اكتشافات سلسلة UBE2M–USP39–PABPC1–CCNB1 إلى نقطة ضعف جديدة في خلايا سرطان القولون والمستقيم. لجأ المؤلفون إلى الميكافنجين (micafungin)، دواء يُستخدم بالفعل لعلاج الالتهابات الفطرية وتم تحديده مؤخرًا كمثبط لنشاط UBE2M في التأشير بالنِدّ. في خلايا سرطان الأمعاء المزروعة في المختبر، أضعف الميكافنجين تأشير USP39 بالنِدّ، وزاد من تحلل PABPC1، وخفض مستويات بروتين CCNB1. ونتيجة لذلك، تباطأ انقسام الخلايا، واحتُجِزت مزيد من الخلايا في نقطة تفتيش G2/M، وزاد الموت المبرمج. في فئران مُزرَعَة بها خلايا سرطان القولون والمستقيم، قلّص العلاج اليومي بالميكافنجين الأورام بشكل كبير مقارنة بالحيوانات غير المعالجة، دون الحاجة إلى إزالة UBE2M نفسه.
ما يعنيه هذا للمرضى على المدى البعيد
ترسم هذه الدراسة صورة واضحة لكيف يمكن لإنزيم واحد، UBE2M، ربط نظام وسم البروتينات الدقيق بقرار خلية سرطان الأمعاء بالانقسام. من خلال استقرار عامل الترجمة (PABPC1) عبر USP39، يرفع UBE2M بشكل غير مباشر مستويات دافع قوي لدورة الخلية، CCNB1، مما يسمح للأورام بالنمو بشكل أسرع. على الرغم من الحاجة لمزيد من الأبحاث والاختبارات السريرية، توحي النتائج بأن تعطيل هذا التتابع — وربما باستخدام أدوية مُعاد توظيفها مثل الميكافنجين — قد يوفر استراتيجية مستهدفة جديدة لإبطاء تقدم سرطان القولون والمستقيم وتحسين نتائج المرضى.
الاستشهاد: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
الكلمات المفتاحية: سرطان القولون والمستقيم, دورة الخلية, التأشير بالنِدّ, UBE2M, العلاج الموجَّه