Clear Sky Science · ar
سُمّية الجهاز الهضمي الناتجة عن الأدوية وسلامة الحاجز: تَضرّر بوساطة الهيكل الخَلَوِي في نموذج بشري معوي ذي صلة سريرية
لماذا تهم الآثار الجانبية المعوية
يمكن للعديد من الأدوية المضادة للسرطان أو الالتهاب أو الأمراض الأخرى أن تضر بطانة أمعائنا عن غير قصد. عندما يتضرر هذا «الجلد» الداخلي للأمعاء، قد يعاني المرضى من إسهال وألم وغثيان وضعف في امتصاص المغذيات، وفي بعض الحالات تكون الأعراض شديدة لدرجة تضطر الأطبَّاء إلى إيقاف أو تقليل علاجات منقذة للحياة. ومع ذلك، غالبًا ما تُفوّت اختبارات المختبر الحالية هذه المشاكل قبل وصول الأدوية إلى المرضى. تُقدّم هذه الدراسة نموذجًا مخبريًا للإنسان المعوي أكثر واقعية وتُظهر كيف يمكنه اكتشاف الأدوية المُسبِّبة لضرر الأمعاء مبكرًا وكشف السبل التي تضعف بها الحاجز الطبيعي للجسم.
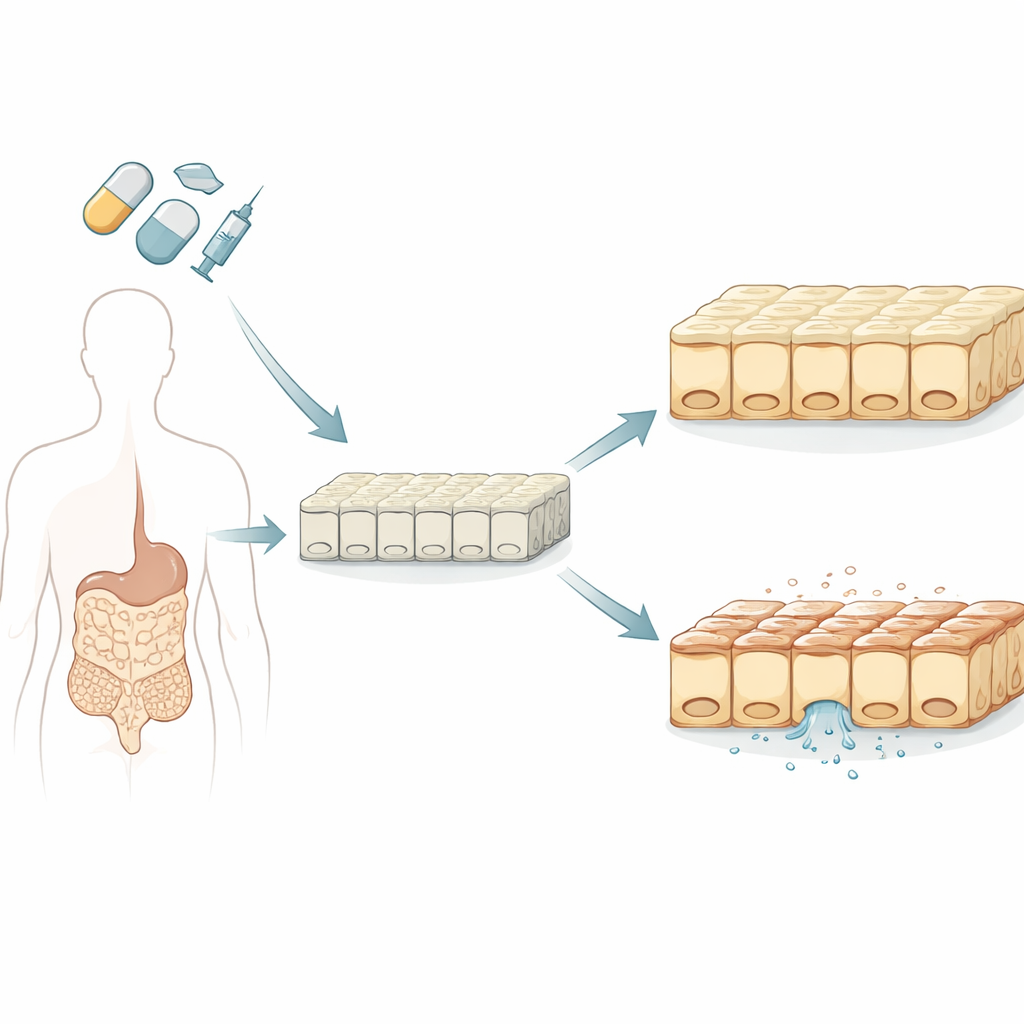
بناء «أمعاء صغيرة» محسنّة
بدأ الباحثون بزراعة صفائح من خلايا الأمعاء البشرية في المختبر باستخدام الخلايا الجذعية، والتي يمكن أن تتطوّر إلى أنواع نسيجية متعددة. على عكس خط الخلايا المأخوذ من السرطان والمستخدم تقليديًا في اختبارات الأدوية، شكّلت الخلايا المشتقة من الخلايا الجذعية مجتمعًا مختلطًا يشبه الأمعاء الدقيقة الحقيقية بشكل أوثق، بما في ذلك خلايا تفرز المخاط وخلايا تنتج الهرمونات. وأكّد الفريق أن هذه البطانة المزروعة في المختبر تملك إحكامًا واقعيًا، واستقطابًا علويًا-سفليًا سليمًا وخصائص نقل واستقلاب رئيسية تؤثر في كيفية مرور الأدوية ومعالجتها في الأمعاء.
قياس الإحكام الكهربائي للحاجز
لاختبار سلامة الأمعاء، ركّز الفريق على مقاومة كهربية عبر الطابق الظهاري (TEER)، وهو مقياس غير غازي لمدى إحكام ارتباط الخلايا المجاورة ببعضها. تعني TEER العالية وجود حاجز محكم ووقائي؛ أما انخفاض TEER فيشير إلى أن الجدار بين الأمعاء والجهاز الدوري أصبح مسريبًا. قارن العلماء قياسات TEER باختبار بقاء الخلية القياسي الذي يقيس جزيئات الطاقة مثل ATP. عرضوا نموذجهم المعوي الجديد ونموذج الخلايا السرطانية القديم لـ 17 دواءً معروفًا بتفاوت معدلات التسبب في آثار معوية، بما في ذلك عوامل العلاج الكيميائي الشائعة وحبوب السرطان الموجهة ومسكنات الألم مثل الإيبوبروفين ومضادات الالتهاب الأخرى.
اكتشاف أضرار خفية قبل موت الخلايا
عبر هذه المجموعة من الأدوية، تفوّق قياس TEER في البطانة المشتقة من الخلايا الجذعية على اختبار ATP التقليدي وحاجز الخلايا السرطانية القديم. أظهرت عدة أدوية كيميائية تغيّراً طفيفًا في مستوى ATP، مما يوحي بأن الخلايا لا تزال على قيد الحياة، ومع ذلك سببت انخفاضات كبيرة في TEER وتلفًا واضحًا في صور تلوين الخلايا الحية/الميتة. هذا يعني أن الحاجز قد يفشل قبل موت الخلايا بالكامل، وهو إنذار مبكر تفوِّته اختبارات الحيوية التقليدية. عندما قارن الفريق نتائج المختبر بسجلات سريرية لمعدلات حدوث الأعراض المعوية لكل دواء، أيّنت اختبار TEER الجديد تحذيرًا صحيحًا لمعظم الأدوية عالية المخاطر وطمأنت بشكل صحيح بشأن الأدوية منخفضة المخاطر، محقِّقًا دقة عالية جدًا.
كيف تقوّض الأدوية الهيكل الداخلي
لاكتشاف ما يحدث داخل الخلايا، حلّل العلماء نشاط الجينات بعد العلاج بعاملين كيميائيين يستهدفان الأنابيب الدقيقة، وهي جزء أساسي من هيكل الخلية الداخلي. وجدوا انخفاضات واسعة في الجينات المشاركة في الهيكل الخلوي، والتلاصق الخلوي، والمصفوفة خارج الخلوية—الشَبكة التي تساعد الخلايا على التثبّت ببيئتها. أظهرت تجارب إضافية زيادات معتمدة على الجرعة في أنواع الأكسجين التفاعلية، وهي جزيئات غير مستقرة تحتوي على الأكسجين يمكن أن تُضرّ بالهياكل الخلوية. تشير هذه التغيرات معًا إلى سلسلة من الأحداث التي تزعزع الإطار الداخلي والروابط بين خلايا الأمعاء، فتُرخّي الحاجز وتسمح بتسرّب المواد بين الخلايا.
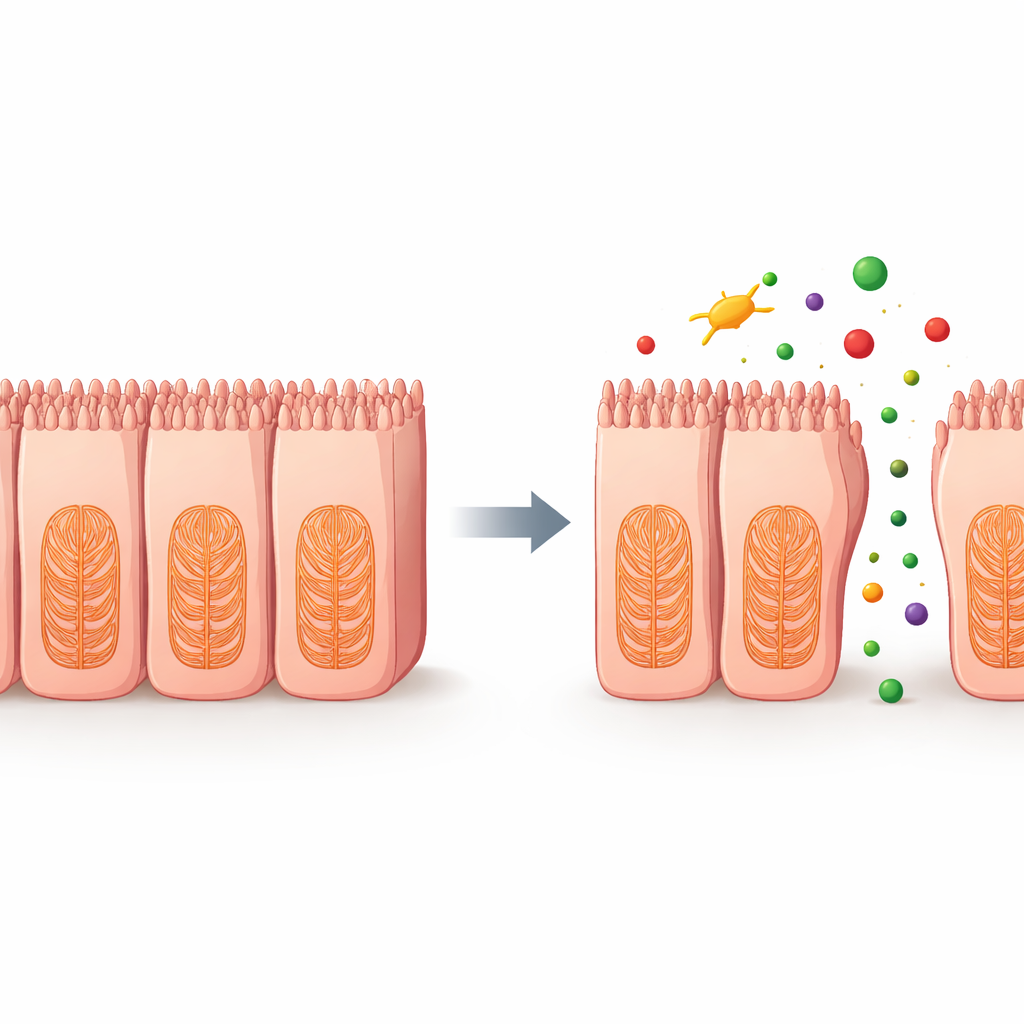
ما يعنيه هذا للمرضى
تُظهر هذه الدراسة أن بطانة معوية بشرية مستمدة من الخلايا الجذعية، مقترنة بقياسات كهربائية بسيطة لإحكام الحاجز، يمكن أن تتنبّأ بشكل أكثر موثوقية بالأدوية المرجّح أن تُسبب إصابة معوية من الطرق المخبرية التقليدية. من خلال كشف ضعف الحاجز مبكرًا وربطه بضرر أساسي في الهيكل الخلوي، قد يساعد هذا النظام مطوِّري الأدوية على استبعاد أو إعادة تصميم المركبات عالية المخاطر قبل وصولها إلى العيادات. وعلى المدى الطويل، قد تقلّل اختبارات «الأمعاء الصغيرة» الواقعية هذه من الآثار المعوية المزعجة أو الخطرة على المرضى، بينما تمكّن الأطباء من استخدام علاجات قوية بأمان أكبر.
الاستشهاد: Yu, W.D., Lee, S., Cho, HS. et al. Drug-induced gastrointestinal toxicity and barrier integrity: cytoskeleton-mediated impairment in a clinically relevant human intestinal epithelium model. Exp Mol Med 58, 487–500 (2026). https://doi.org/10.1038/s12276-025-01635-6
الكلمات المفتاحية: سُمّية الجهاز الهضمي, حاجز الأمعاء, نموذج الخلايا الجذعية, سلامة الأدوية, آثار جانبية للعلاج الكيميائي