Clear Sky Science · ar
رمزان لتحرير الحمض النووي الريبي عن طريق نزع الأمين في الأمراض البشرية
كيف تعيد الخلايا كتابة رسائلها
كل خلية في جسمك تقرأ باستمرار تعليمات من الحمض النووي لبنائك والحفاظ عليك. لعقود افترضنا أن هذه التعليمات تُنسخ إلى الحمض النووي الريبي ثم تُترجم بأمانة إلى بروتينات. تُظهر هذه المراجعة أن القصة أقل صلابة بكثير: فالخلايا في الواقع "تعيد كتابة" العديد من رسائل الحمض النووي الريبي بعد تكوينها، مستبدلة حروفًا كيميائية مفردة بطرق قد تغير بشكل طفيف أو جذري كيفية عمل أجسامنا. يساعد فهم هذه الطبقة الخفية من التحرير في تفسير سبب إصابة الأشخاص بأمراض مناعية ذاتية، واضطرابات عصبية، ومشكلات أيضية، وعدوى وسرطان — وكيف قد نعالجها في النهاية.
طريقتان لتغيير حرف واحد
يركز المؤلفون على نوعين رئيسيين من تحرير الحمض النووي الريبي الموجودين لدى البشر. الأول يُسمى تحرير A‑إلى‑I، وتقوم به إنزيمات تعرف باسم ADARs. تغير هذه الإنزيمات القاعدة أدينوسين (A) إلى إينوزين (I)، والذي تقرأه آليات الخلية في الغالب كما لو كان غوانين (G). الثاني هو تحرير C‑إلى‑U، الذي تقوم به إنزيمات عائلة APOBEC، والتي تحول السيتيدين (C) إلى يوريدين (U). كلا العمليتين تزيلان مجموعة كيميائية صغيرة من قاعدة واحدة، لكنهما تختلفان في أين تعملان، وأي أنواع الحمض الريبي تفضّلان، ومدى تأثيرهما على بنية الحمض الريبي. غالبًا ما يغير تحرير A‑إلى‑I كيفية اقتران سلاسل الحمض الريبي ويمكن أن ينوّع البروتينات أو يغيّر كيفية ارتباط جزيئات أخرى بالحمض الريبي. يميل تحرير C‑إلى‑U إلى أن يكون أكثر دقة من الناحية البنيوية، ولكنه لا يزال قادرًا على إدخال إشارات إيقاف، أو تعديل تسلسل البروتينات، أو ضبط المناطق التنظيمية من الحمض الريبي.
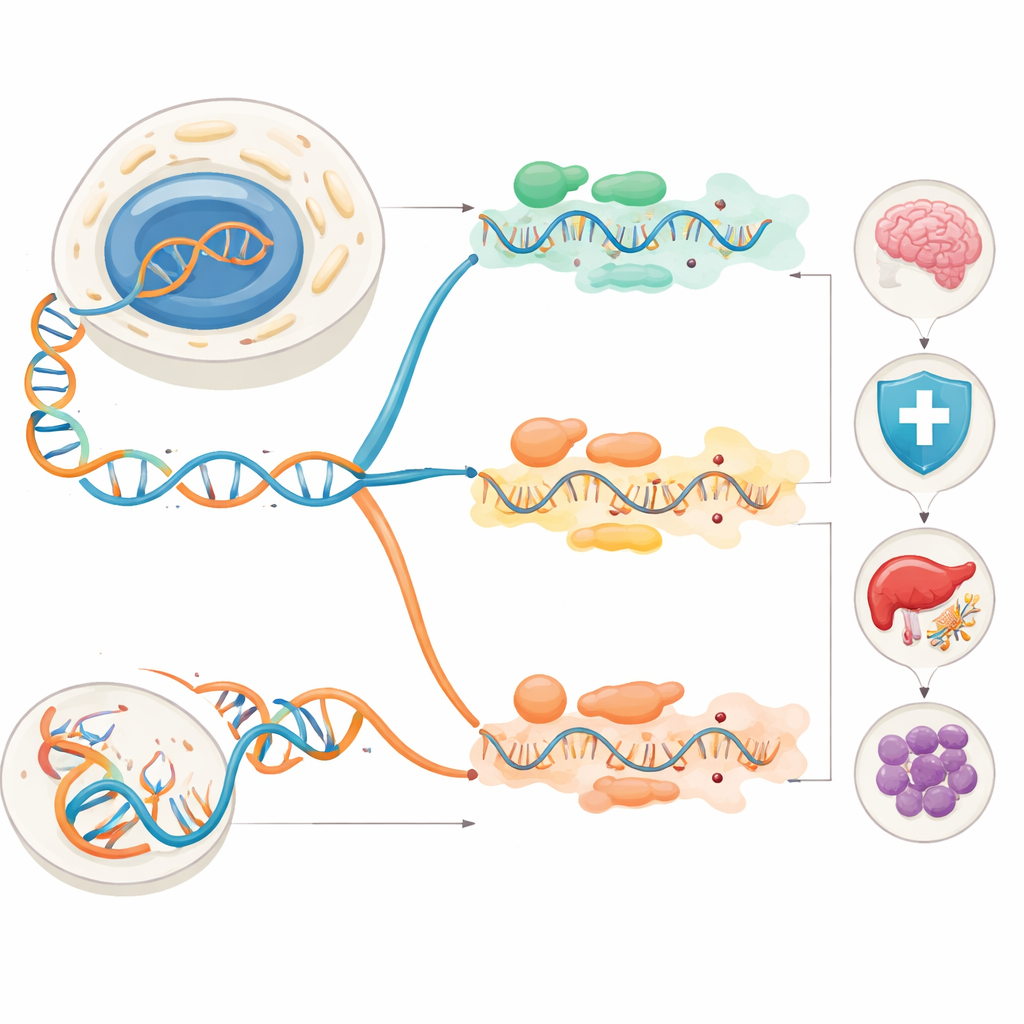
من الرسائل المعدّلة إلى الصحة والمرض
نظرًا لأن هذه التعديلات يمكن أن تغيّر أجزاء من البروتين أو المناطق التنظيمية المحيطة بها، فإنها تمس العديد من جوانب البيولوجيا الطبيعية. في الجهاز المناعي، يقوم ADAR1 بتحرير الحمض الريبي مزدوج السلسلة المُنتَج ذاتيًا حتى لا تخلطه مجسات الفيروسات مع دخيل أجنبي. عندما يفشل ADAR1، تبقى إنذارات المناعة في حالة "تشغيل" مستمر، مما يؤدي إلى إشارة إنترفيرون مزمنة وحالات مناعية ذاتية مثل متلازمة أيكاري–غوتييريس. كما تقوم إنزيمات APOBEC بتحرير الحمض الريبي في الخلايا المناعية، مشكِّلة كيفية استجابة البلاعم للإجهاد والالتهاب وقد تساهم في أمراض مثل الذئبة الحمامية الجهازية. في الجهاز العصبي، يُعد تحرير ADAR2 حاسمًا لضبط مستقبلات المخ التي تتحكم في تدفق الكالسيوم؛ وبدونه تعاني الفئران من نوبات وتموت مبكرًا. قد يزيد تحرير APOBEC لبعض حمضيات المستقبلات في الخلايا العصبية من حساسيتها ويرتبط بالصرع والتنكس والمشكلات الإدراكية.
الفيروسات والأيض وصلة السرطان
يؤثر تحرير الحمض الريبي أيضًا على كيفية تفاعلنا مع الفيروسات، وإدارة الطاقة، وتطور السرطان. يمكن أن يحرر ADAR1 الجينومات الفيروسية مباشرةً، أحيانًا معطلاً الفيروس وأحيانًا، كما في فيروس التهاب الكبد دلتا، مساعدًا إياه على إكمال دورة حياته. تُعرف إنزيمات APOBEC بهجومها على الفيروسات الراجعة، وتترك بصمة قوية من نوع C‑إلى‑U في حمض SARS‑CoV‑2 الريبي، مما يحد أحيانًا من الفيروس وفي الوقت نفسه يولّد طفرات قد تساعد على تطوره. في الأيض، يساعد ADAR2 خلايا بيتا البنكرياسية على ضبط إفراز الإنسولين استجابة للنظام الغذائي، بينما تؤثر نشاطات ADAR1 وADAR2 على خطر الإصابة بالسكري ومرض الكبد الدهني. الدور الكلاسيكي لـ APOBEC1 هو تحرير الحمض الريبي لأبوليبوبروتين ب، مما ينتج بروتينًا مختصرًا أساسيًا لنقل الدهون الغذائية؛ عندما يفقد هذا التحرير، تتطور لدى الفئران مشكلات خطيرة في الدهون والكوليسترول.
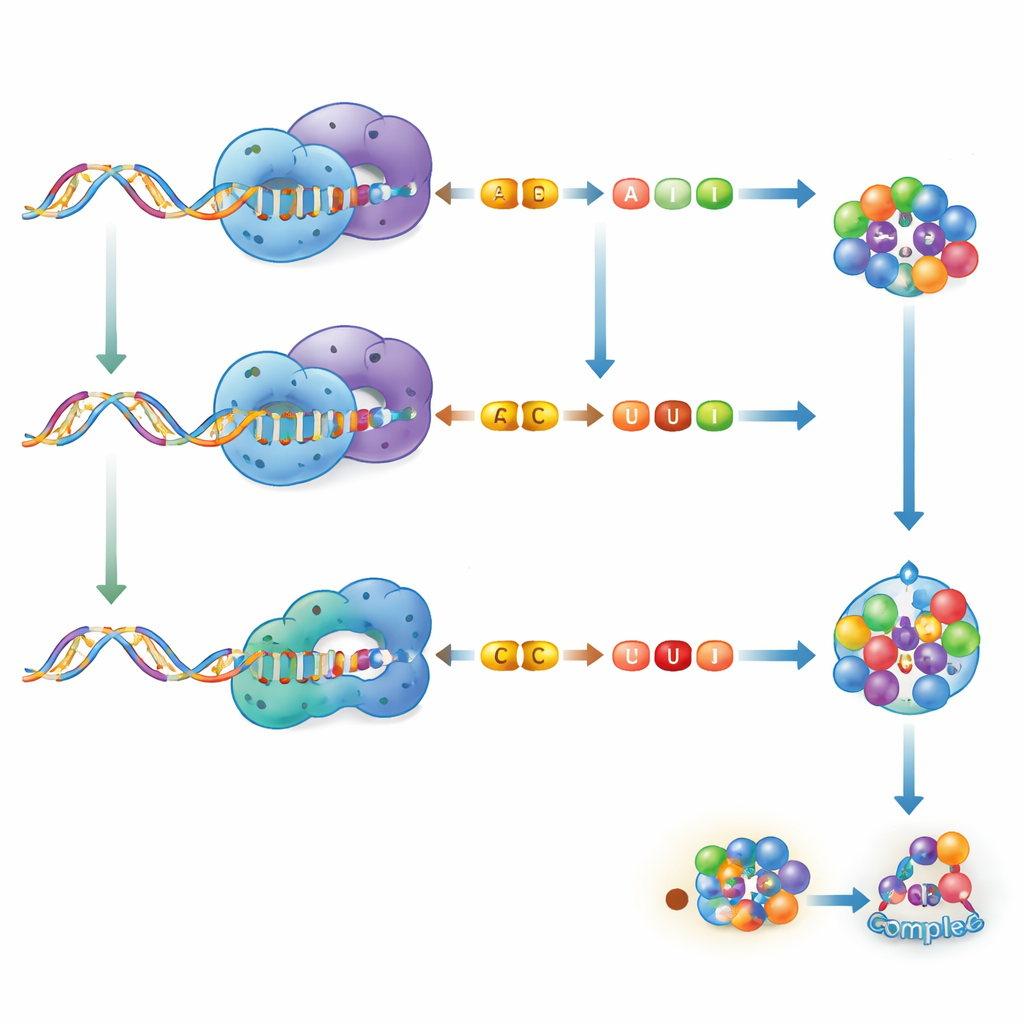
كيف يشكل الحمض الريبي المحرر الأورام
يمكن لأنفس الإنزيمات التي تحمينا أن تدفع نحو السرطان عند تنظيمها بشكل خاطئ. كشفت مشاريع ترميز السرطان الكبيرة عن عشرات الآلاف من مواقع تحرير A‑إلى‑I وانتشار طفرات مرتبطة بـ APOBEC. في سرطان الثدي، قد يحفز تحرير ADAR1 أو يكبح سلوك الورم اعتمادًا على الحمض الريبي المستهدف، مما يؤثر على غزو الخلايا والانتشار والبقاء. في الورم الأرومي الدبقي، وهو ورم دماغي قاتل، يدعم ADAR1 الخلايا الجذعية السرطانية، بينما يعمل ADAR2 عمومًا كفرامل للنمو عن طريق تحرير كل من حمضيات ترمز لبروتينات وميكرو‑RNA التي تروّج للسرطان. في اللوكيميا، غالبًا ما يعزز ADAR1 خلايا شبيهة بالجذعية الخبيثة ويخمد ميكرو‑RNA المثبط للورم، بينما يحرر ADAR2 أهدافًا محددة بطرق تبطيء المرض. يمكن لتحرير C‑إلى‑U بوساطة APOBEC لبعض الحمضيات في سرطانات الدم أن يفاقم أو يحسّن نتائج المرضى، مما يبرز الطابع المعتمد على السياق لهذه التغيرات.
أسئلة بلا إجابة وإمكانات مستقبلية
رغم الطفرة في قوائم مواقع التحرير الموثقة، لا يزال العلماء يكافحون لتمييز التعديلات ذات المغزى عن الضوضاء الخلفية. قد يكون للعديد من التغييرات المكتشفة تأثير ضئيل، لكن قلة منها بوضوح لها عواقب قد تكون مسألة حياة أو موت للخلايا والكائنات الحية. يجادل المؤلفون بأن العمل المستقبلي يجب أن يحدد أية إنزيمات وبروتينات مساعدة تتحكم في مواقع فردية، ثم يختبر ماذا يحدث عندما يُجبَر ذلك الحرف الواحد ليكون محررًا دائمًا أو غير محرر أبدًا. ستوضح مثل هذه الدراسات كيف يساهم تحرير الحمض الريبي في أمراض محددة وتكشف ما إذا كان تعديل أنماط التحرير يمكن أن يصبح فئة جديدة من العلاجات الدقيقة — لتهدئة جهاز مناعي مفرط النشاط، أو ضبط دوائر المخ، أو تصحيح اختلالات أيضية، أو جعل السرطانات أكثر عرضة للعلاج.
لماذا يهم هذا للصحة اليومية
بعبارات بسيطة، تُظهر هذه المقالة أن خلايانا لا تكتفي بقراءة الشفرة الجينية؛ بل تقوم بتدقيقها ومراجعتها بنشاط على مستوى الحمض الريبي، مستخدمة رمزين موازيين لـ "التحرير". عندما تحدث هذه التعديلات الصغيرة في المكان والكمية الصحيحين، فإنها تساعد على إبقاء جهازنا المناعي متوازنًا، وأدمغتنا مستقرة، وأيضتنا مرنة، ودفاعاتنا ضد الفيروسات حادة. عندما يكون جهاز التحرير مفرط النشاط أو منحرفًا أو معطلاً، يمكن لتلك التغييرات نفسها أن تقودنا نحو المناعة الذاتية، أو العدوى، أو الخرف، أو المرض الأيضي أو السرطان. من خلال رسم خرائط وفهم هذه عمليات إعادة الكتابة لحرف واحد، يأمل العلماء في تشخيص المرض مبكرًا، وتوقع من هو في خطر، وتصميم علاجات تدفع عملية التحرير نحو حالة صحية.
الاستشهاد: Min, D.J., Lee, S., Lee, Ys. et al. Two codes of RNA editing by deamination in human diseases. Exp Mol Med 58, 382–395 (2026). https://doi.org/10.1038/s12276-025-01633-8
الكلمات المفتاحية: تحرير الحمض النووي الريبي, ADAR, APOBEC, الذاتية المناعة, السرطان